题目内容
5.某兴趣小组为检验泻盐中是否含有SO42-,选用稀盐酸和BaCl2溶液进行探究,其中稀盐酸的作用是排除某杂质离子的干扰,该杂质离子是( )| A. | Ag+ | B. | Ca2+ | C. | CO${\;}_{3}^{2-}$ | D. | NO${\;}_{3}^{-}$ |
分析 检验SO42-,选用稀盐酸和BaCl2溶液,因硫酸钡、氯化银均为不溶于酸的白色沉淀,则先加盐酸排除干扰离子,以此来解答.
解答 解:检验泻盐中是否含有SO42-,因Ag+与Cl-结合生成白色沉淀,CO32-与Ba2+结合生成白色沉淀,则先加稀盐酸的作用是排除Ag+、CO32-等离子的干扰,再加BaCl2溶液,生成白色沉淀,可说明含SO42-,
故选AC.
点评 本题考查常见离子的检验,为高频考点,把握离子检验的试剂、现象、结论为解答的关键,侧重分析与实验能力的考查,注意排除干扰离子的影响,题目难度不大.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
15.有一包铁粉和铜粉混合均匀的粉末样品,为确定其组成,某同学将不同质量的该样品分别与40mL1mol/L的FeCl3溶液反应,实验结果如表所示(忽略反应前后溶液体积的微小变化).
(1)实验四的滤液中c(Fe2+)=1.5 mol/L.
(2)原粉末样品中m(Fe):m(Cu)=7:8.
| 实验序号 | ① | ② | ③ | ④ |
| M(粉末样品)/g | 0.90 | 1.80 | 3.60 | 7.20 |
| M(反应后剩余固体)/g | 0 | 0.64 | 2.48 | 6.08 |
(2)原粉末样品中m(Fe):m(Cu)=7:8.
16.下列各图曲线分别表示物质的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质),下列选项中的对应关系错误的是( )
| A. |  图可以表示Si、P、S、Cl四种元素的最低负化合价的绝对值 | |
| B. | 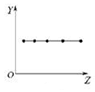 图可以表示ⅡA族元素的原子最外层电子数 | |
| C. |  图可以表示ⅥA族元素气态氢化物的稳定性 | |
| D. | 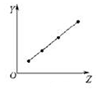 图可以表示第三周期非金属元素的最高价氧化物对应水化物的酸性 |
20.一定质量的铁与足量稀硫酸反应制氢气,下列措施能加快氢气生成速率,但不能影响生成氢气的量的是( )
| A. | 滴加CuSO4溶液 | B. | 选用质量分数为98%的浓硫酸 | ||
| C. | 不用铁片,改用等质量的铁粉 | D. | 增加稀硫酸的体积 |
10.下列实验操作中现象以及结论不正确的是( )
| 实验操作 | 现象 | 结论 | |
| A | 将干燥纯净的氯气通入装有湿润的红色纸条的试剂瓶中 | 纸条褪色 | 氯气有漂白性 |
| B | 将一定量的浓硫酸加入蔗糖 | 固体变黑膨胀 | 浓硫酸有吸水性和强氧化性 |
| C | 向酸性KMnO4溶液中通入SO2气体 | KMnO4溶液褪色 | SO2有还原性 |
| D | 金属钠投入CuSO4溶液 | 析出红色固体 | 钠的金属性比铜强 |
| A. | A | B. | B | C. | C | D. | D |
17.柠檬烯是一种食用香料,其结构简式如图所示.下列有关柠檬烯的分析正确的是( )

| A. | 它的一氯代物有6种 | |
| B. | 它的分子中所有的碳原子一定在同一平面上 | |
| C. | 它和丁基苯( )互为同分异构体 )互为同分异构体 | |
| D. | 一定条件下,它分别可以发生加成、取代、氧化、还原等反应 |
14.用铁片与稀硫酸反应制取氢气时,下列措施不能使生成氢气的速率加大的是( )
①加热
②不用稀硫酸,改用98%的浓硫酸
③增加同浓度稀硫酸的用量
④不用铁片,改用铁粉
⑤滴加几滴CuSO4溶液.
①加热
②不用稀硫酸,改用98%的浓硫酸
③增加同浓度稀硫酸的用量
④不用铁片,改用铁粉
⑤滴加几滴CuSO4溶液.
| A. | ①②③④⑤ | B. | ①③⑤ | C. | ②③ | D. | ③④ |
15. 常温下,向100mL0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中正确的是( )
常温下,向100mL0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中正确的是( )
 常温下,向100mL0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中正确的是( )
常温下,向100mL0.01mol•L-1HA溶液中逐滴加入0.02mol•L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计).下列说法中正确的是( )| A. | MOH为一元强碱HA为一元强酸 | |
| B. | K 点对应的溶液中:c(M+)+c(MOH)=c(A-) | |
| C. | K点对应的溶液中:c(MOH)+c(OH-)-c(H+)=0.005mol•L-1 | |
| D. | N点水的电离程度小于K点水的电离程度 |