题目内容
【题目】某学生探究![]() 溶液与
溶液与![]() 溶液的反应,实验如下:
溶液的反应,实验如下:
实验1 |
|
实验2 |
|
下列分析不正确的是( )
A.白色沉淀![]() 、
、![]() 都是含铝化合物
都是含铝化合物
B.白色沉淀的![]() 与稀硫酸反应时有
与稀硫酸反应时有![]() 气体生成
气体生成
C.白色沉淀![]() 、
、![]() 的成分不同,洗涤时要检验是否洗涤干净必须用不同的试剂
的成分不同,洗涤时要检验是否洗涤干净必须用不同的试剂
D.实验1、2中白色沉淀成分不同可能与混合后溶液的![]() 有关
有关
【答案】C
【解析】
实验1在过量的硫酸铝溶液中加入碳酸钠溶液,过滤、洗涤,得到的沉淀a加入稀硫酸,沉淀溶解,没有气泡,可说明沉淀a为Al(OH)3;实验2在过量的碳酸钠溶液中加入硫酸铝溶液,过滤、洗涤,得到沉淀b,加入稀硫酸,沉淀溶解,并有少量气泡,沉淀b中含碳酸根、且其阳离子有Al3+。
A.沉淀a加入稀硫酸,沉淀溶解,没有气泡,可说明沉淀a为Al(OH)3;沉淀b加入稀硫酸,沉淀溶解,并有少量气泡,沉淀b中含碳酸根、且其阳离子有Al3+,所以白色沉淀![]() 、
、![]() 都是含铝化合物,故A正确;
都是含铝化合物,故A正确;
B.白色沉淀![]() 与稀硫酸反应时有气体生成,该气体为二氧化碳,故B正确;
与稀硫酸反应时有气体生成,该气体为二氧化碳,故B正确;
C.检验沉淀是否洗涤干净,可检验最后一次洗涤液中是否含有硫酸根离子,即向最后一次洗涤液中滴加盐酸酸化的BaCl2溶液,观察是否有沉淀生成,故C错误;
D.实验1中硫酸铝溶液过量,溶液呈酸性,实验2中碳酸钠溶液过量,溶液呈碱性,生成沉淀时溶液的pH不同,生成的沉淀不同,可说明沉淀成分不同与pH有关,故D正确;
选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下列表格中的各种情况,可以用右图的曲线表示的是 ( )
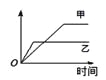
反 应 | 纵坐标 | 甲 | 乙 | |
A | 相同质量的氨,在同一容器中 | 氨气的转化率 | 500℃ | 400℃ |
B | 等质量钾、钠分别与足量水反应 | H2质量 | 钠 | 钾 |
C | 在体积可变的恒压容器中,体积比1︰3的N2、H2, | 氨气的浓度 | 活性高的催化剂 | 活性一般的催化剂 |
D | 2 molSO2和1 molO2,在相同温度下2SO2+ O2 | SO3物质的量 | 2个大气压 | 10个大气压 |
A. AB. BC. CD. D