题目内容
将不同量的CO(g)和H2O(g)分别通入体积为2L的恒容密闭容器中,进行反应:CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| H2O | CO | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 3 |
| 3 | 900 | 1 | 2 | 0.4 | 1 |
(2)该反应的正反应为______(填“吸”或“放”)热反应.
(3)计算650℃时该反应的平衡常数K(650℃)=______;估计900℃时该反应的平衡
常数K(900℃)______(填“>”、“<”或“=”)K(650℃).
(4)实验3跟实验2相比,改变的条件可能是______.
(5)下列事实能说明该反应达到平衡的有______(填序号).
①容器内压强不再改变 ②容器内气体密度不再改变
③容器内H2O的质量不再改变 ④v正(H2)=v逆(CO)
⑤反应热不再改变.
【答案】分析:(1)根据方程式可知v(H2)=v(CO2),根据v=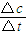 计算;
计算;
(2)第二组温度比第一组高,反应物物质的量比第一组减半,但是平衡时CO2的物质的量比第一组的一半少,表明该反应为放热反应;
(3)首先计算出平衡时各物质的浓度,根据K=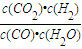 计算,结合温度对平衡移动的影响判断;
计算,结合温度对平衡移动的影响判断;
(4)实验3跟实验2相比,温度相同,浓度相同,但实验3达到平衡所用时间少,反应速率更大,但平衡状态一样;
(5)结合反应的方程式的特点,到达平衡时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量也不变.
解答:解:(1)根据方程式可知v(H2)=v(CO2),则v(H2)=v(CO2)=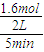 =0.16mol/(L?min),故答案为:0.16mol/(L?min);
=0.16mol/(L?min),故答案为:0.16mol/(L?min);
(2)实验1中CO的转化率为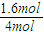 ×100%=40%,实验2中CO的转化率为
×100%=40%,实验2中CO的转化率为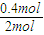 ×100%=20%,则实验1的转化率大于实验2,则说明温度升高平衡向逆反应方向移动,正反应放热,
×100%=20%,则实验1的转化率大于实验2,则说明温度升高平衡向逆反应方向移动,正反应放热,
故答案为:放;
(3)H2O(g)+CO(g) CO2(g)+H2(g)
CO2(g)+H2(g)
初始 1mol/L 2mol/L 0 0
转化 0.8mol/L 0.8mol/l 0.8mol/l 0.8mol/l
平衡 0.2mol/L 1.2mol/L 0.8mol/l 0.8mol/l
根据K=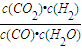 计算可得该反应在650℃时平衡常数数值为K=
计算可得该反应在650℃时平衡常数数值为K=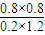 =
= =2.67,
=2.67,
该反应的正反应放热,升高温度平衡向逆反应方向移动,则平衡常数减小,
故答案为:2.67;<;
(4)实验3跟实验2相比,温度相同,浓度相同,但实验3达到平衡所用时间少,反应速率更大,但平衡状态一样,应是使用了催化剂,由于反应前后气体体积不变,则增大了压强,平衡也不移动,也可能为压强的增大,
故答案为:使用了催化剂或增大了压强;
(5)①由于反应前后气体的体积不变,则无论是否达到平衡状态都存在容器内压强不改变,不能作为判断达到平衡的依据,故①错误;
②由于气体的质量不变,容器的体积不变,则无论是否达到平衡状态,容器内气体密度都不变,不能作为判断达到平衡的依据,故②错误;
③容器内H2O的质量不再改变,说明达到平衡状态,故③正确;
④v正(H2)=v逆(CO),说明正逆反应速率相等,达到平衡状态,故④正确;
⑤无论是否达到平衡状态,反应热都不变,不能作为达到平衡状态的依据,因为反应热只与反应物的起始状态和终态有关,故⑤错误.
故答案为:③④.
点评:本题考查化学平衡的计算,题目难度中等,做题时注意把握影响平衡移动的因素以及平衡常数的有关计算,此为化学平衡常考查问题.
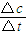 计算;
计算;(2)第二组温度比第一组高,反应物物质的量比第一组减半,但是平衡时CO2的物质的量比第一组的一半少,表明该反应为放热反应;
(3)首先计算出平衡时各物质的浓度,根据K=
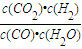 计算,结合温度对平衡移动的影响判断;
计算,结合温度对平衡移动的影响判断;(4)实验3跟实验2相比,温度相同,浓度相同,但实验3达到平衡所用时间少,反应速率更大,但平衡状态一样;
(5)结合反应的方程式的特点,到达平衡时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量也不变.
解答:解:(1)根据方程式可知v(H2)=v(CO2),则v(H2)=v(CO2)=
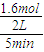 =0.16mol/(L?min),故答案为:0.16mol/(L?min);
=0.16mol/(L?min),故答案为:0.16mol/(L?min);(2)实验1中CO的转化率为
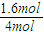 ×100%=40%,实验2中CO的转化率为
×100%=40%,实验2中CO的转化率为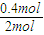 ×100%=20%,则实验1的转化率大于实验2,则说明温度升高平衡向逆反应方向移动,正反应放热,
×100%=20%,则实验1的转化率大于实验2,则说明温度升高平衡向逆反应方向移动,正反应放热,故答案为:放;
(3)H2O(g)+CO(g)
 CO2(g)+H2(g)
CO2(g)+H2(g)初始 1mol/L 2mol/L 0 0
转化 0.8mol/L 0.8mol/l 0.8mol/l 0.8mol/l
平衡 0.2mol/L 1.2mol/L 0.8mol/l 0.8mol/l
根据K=
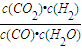 计算可得该反应在650℃时平衡常数数值为K=
计算可得该反应在650℃时平衡常数数值为K=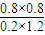 =
= =2.67,
=2.67,该反应的正反应放热,升高温度平衡向逆反应方向移动,则平衡常数减小,
故答案为:2.67;<;
(4)实验3跟实验2相比,温度相同,浓度相同,但实验3达到平衡所用时间少,反应速率更大,但平衡状态一样,应是使用了催化剂,由于反应前后气体体积不变,则增大了压强,平衡也不移动,也可能为压强的增大,
故答案为:使用了催化剂或增大了压强;
(5)①由于反应前后气体的体积不变,则无论是否达到平衡状态都存在容器内压强不改变,不能作为判断达到平衡的依据,故①错误;
②由于气体的质量不变,容器的体积不变,则无论是否达到平衡状态,容器内气体密度都不变,不能作为判断达到平衡的依据,故②错误;
③容器内H2O的质量不再改变,说明达到平衡状态,故③正确;
④v正(H2)=v逆(CO),说明正逆反应速率相等,达到平衡状态,故④正确;
⑤无论是否达到平衡状态,反应热都不变,不能作为达到平衡状态的依据,因为反应热只与反应物的起始状态和终态有关,故⑤错误.
故答案为:③④.
点评:本题考查化学平衡的计算,题目难度中等,做题时注意把握影响平衡移动的因素以及平衡常数的有关计算,此为化学平衡常考查问题.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案
相关题目
 汽车尾气已成为重要的空气污染物.
汽车尾气已成为重要的空气污染物.(1)汽车内燃机工作时引起反应:N2(g)+O2(g)=2NO(g),是导致汽车尾气中含有NO的原因之一.T℃时,向5L密闭容器中充入8mol N2和9molO2,5min后达平衡时NO 物质的量为6mol,该反应的速率v(NO)为
(2)H2或CO可以催化还原NO以达到消除污染的目的:
①已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol
则H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式为
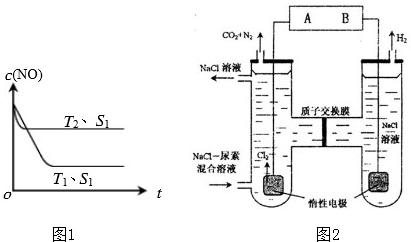
②当质量一定时,增大固体催化剂的表面积可提高化学反应速率.如图1是反应:
2NO(g)+2CO(g)=2CO2(g)+N2(g)中NO的浓度随温度(T)、催化剂表面积(S)和时间(t)的变化曲线,据此判断该反应的△H
(3)人工肾脏可用间接电化学方法除去代谢产物中的尿素(CO(NH2)2),即通过阳极反应生成具有强氧化作用的中间产物来氧化代谢产物,原理如图2:
①电源的负极为
②阳极室中发生的反应为
③电解结束后,阴极室溶液的pH与电解前相比将
(4)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组数据:
| 实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需 时间/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
②实验3中,若平衡时,CO的转化率大于水蒸气的转化率,则
| a |
| b |
③实验4,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时V正
 (2013?上饶一模)“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题
(2013?上饶一模)“低碳循环”引起各国的高度重视,而如何降低大气中CO2的含量及有效地开发利用CO2,引起了全世界的普遍重视.所以“低碳经济”正成为科学家研究的主要课题