��Ŀ����
. (10��)����������ѧ��Ӧ��ƽ�ⳣ����K1��K2��K3�����¶ȵĹ�ϵ�ֱ����±���ʾ��

��ش�
(1)��Ӧ���� ������ȡ����ȡ�����Ӧ��
(2)д����Ӧ�۵�ƽ�ⳣ��K3�ı���ʽ ��
(3)���ݷ�Ӧ����ڿ��Ƶ���K1��K2��K3֮��Ĺ�ϵ����K3= ����K1��K2��ʾ����
(4)Ҫʹ��Ӧ����һ�������½�����ƽ�����淴Ӧ�����ƶ����ɲ�ȡ�Ĵ�ʩ��
________(��д��ĸ���)��
E���跨��Сƽ����ϵ�е�CO��Ũ��
(5)����Ӧ�۵��淴Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ��

�ٿɼ���Ӧ��t1��t3��t7ʱ���ﵽ��ƽ�⣬��t2��t8ʱ���ı���һ�����������жϸı����ʲô������t2ʱ__________________��t8ʱ__________________��
����t4ʱ��ѹ�� t6ʱ����Ӧ���Ũ�ȣ�����ͼ�л���t4��t6ʱ�淴Ӧ������ʱ
��Ĺ�ϵ�ߡ�

��ش�
(1)��Ӧ���� ������ȡ����ȡ�����Ӧ��
(2)д����Ӧ�۵�ƽ�ⳣ��K3�ı���ʽ ��
(3)���ݷ�Ӧ����ڿ��Ƶ���K1��K2��K3֮��Ĺ�ϵ����K3= ����K1��K2��ʾ����
(4)Ҫʹ��Ӧ����һ�������½�����ƽ�����淴Ӧ�����ƶ����ɲ�ȡ�Ĵ�ʩ��
________(��д��ĸ���)��
| A����С��Ӧ�������ݻ� |
| B������Ӧ�������ݻ� |
| C�������¶� |
| D��ʹ�ú��ʵĴ��� |
(5)����Ӧ�۵��淴Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ��

�ٿɼ���Ӧ��t1��t3��t7ʱ���ﵽ��ƽ�⣬��t2��t8ʱ���ı���һ�����������жϸı����ʲô������t2ʱ__________________��t8ʱ__________________��
����t4ʱ��ѹ�� t6ʱ����Ӧ���Ũ�ȣ�����ͼ�л���t4��t6ʱ�淴Ӧ������ʱ
��Ĺ�ϵ�ߡ�

���⿼�黯ѧ��Ӧ���ʡ���ѧƽ��������⡣��1����Ӧ���¶����ߣ�K����ƽ���������ƶ���������Ӧ����Ϊ���ȡ���2��K3=����3��K1=��K2=��K3==����4���÷�ӦΪ�������ķ�Ӧ���ı��������ʹƽ���ƶ�����A��B���У����ݣ�3���ɵ�K3(973K)= ="1.62" ��K3(1173K)= =0.78�������¶�ƽ���������ƶ�����C���ԣ�����������ƽ���ƶ�����D���У���СCOŨ�ȣ�����С��ӦŨ�ȣ�ƽ�������ƶ���E���ԡ���5��t2ʱ���淴Ӧ����ͻȻ����Ȼ���С��ƽ�������ƶ��������������¶Ȼ�������������Ũ�ȣ�t8ʱ���淴Ӧ���ʣ�ͻȻ����ƽ��û�з����ƶ�����Ϊʹ�ã���������������ѹǿ��t4ʱ������ѹǿ�����ʼ�С��ƽ�ⲻ�ƶ���

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
 Ca5(PO4)3OH���̣�
Ca5(PO4)3OH���̣� 5Ca2++3PO43-+OH-
5Ca2++3PO43-+OH- 2HI��g������H��0������ͬ�ݻ����ܷ��������ң����м���H2��I2��0��1mol�����м���0��1mol H2��0��2molI2����ͬ�¶��·ֱ�ﵽƽ�⡣����˵������ȷ����
2HI��g������H��0������ͬ�ݻ����ܷ��������ң����м���H2��I2��0��1mol�����м���0��1mol H2��0��2molI2����ͬ�¶��·ֱ�ﵽƽ�⡣����˵������ȷ���� CH3OH(g) ��H
CH3OH(g) ��H

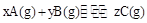
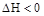 ���ﵽ��ѧƽ�����A�����Ũ��Ϊ
���ﵽ��ѧƽ�����A�����Ũ��Ϊ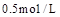 ���������½��ܱ��������ݻ�����һ�����ٴδﵽƽ��ʱ�����A�����Ũ��Ϊ
���������½��ܱ��������ݻ�����һ�����ٴδﵽƽ��ʱ�����A�����Ũ��Ϊ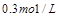 ��������������ȷ���ǣ� ��
��������������ȷ���ǣ� ��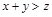
 cZ(g)��?H��0�����ȷ�Ӧ�����ڲ�ͬ�¶�(T1��T2)��ѹǿ(P1��P2)�£�����Z�����ʵ���(nz)�뷴Ӧʱ��(t)�Ĺ�ϵ��ͼ��ʾ.�����ж���ȷ���ǣ�
cZ(g)��?H��0�����ȷ�Ӧ�����ڲ�ͬ�¶�(T1��T2)��ѹǿ(P1��P2)�£�����Z�����ʵ���(nz)�뷴Ӧʱ��(t)�Ĺ�ϵ��ͼ��ʾ.�����ж���ȷ���ǣ�
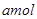
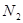 ��
��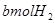 �Ļ������ͨ��һ���̶��ݻ����ܱ������У��������·�Ӧ��
�Ļ������ͨ��һ���̶��ݻ����ܱ������У��������·�Ӧ��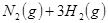

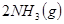
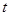 ʱ��
ʱ��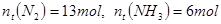 ����a=_______��
����a=_______��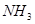 �ĺ��������������Ϊ25%��ƽ��ʱ
�ĺ��������������Ϊ25%��ƽ��ʱ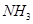 �����ʵ���__________��
�����ʵ���__________��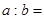 __________��
__________��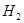 ��ת����֮�ȣ�
��ת����֮�ȣ�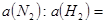 __________��
__________�� 2B(g)+C(g)����H>0����ƽ��ʱ��ҪʹV���������͡�C(A)����Ӧ��ȡ�Ĵ�ʩ�ǣ� ��
2B(g)+C(g)����H>0����ƽ��ʱ��ҪʹV���������͡�C(A)����Ӧ��ȡ�Ĵ�ʩ�ǣ� ��