题目内容
1.下列物质的电子式书写正确的是( )| A. | N2的电子式: | B. | Na2O2的电子式: | ||
| C. | CO2的电子式: | D. | NH4Cl的电子式: |
分析 A.N原子满足8电子稳定结构;
B.为离子化合物,含离子键;
C.C与O之间形成2对共用电子对;
D.为离子化合物,含N-H共价键,阴离子用中括号并标电荷.
解答 解:A.氮气分子中存在氮氮三键,氮原子最外层为8个电子,氮气正确的电子式为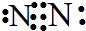 ,故A错误;
,故A错误;
B.Na2O2是钠离子和过氧根离子构成的离子化合物,电子式为 ,故B错误;
,故B错误;
C.CO2是共价化合物,C、O之间形成两对共用电子对,电子式为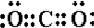 ,故C错误;
,故C错误;
D.NH4Cl为离子化合物,含离子键和共价键,其电子式为 ,故D正确;
,故D正确;
故选D.
点评 本题考查常见化学用语的表示方法,为高频考点,把握电子式的书写、化合物中的化学键为解答的关键,侧重分析与应用能力的考查,注意化学用语的规范使用,题目难度不大.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
11.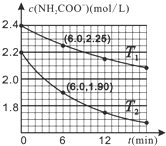 已知:NH2COO-+2H2O═HCO3-+NH3˙H2O.现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是( )
已知:NH2COO-+2H2O═HCO3-+NH3˙H2O.现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是( )
 已知:NH2COO-+2H2O═HCO3-+NH3˙H2O.现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是( )
已知:NH2COO-+2H2O═HCO3-+NH3˙H2O.现用两份氨基甲酸铵溶液在不同温度(T1和T2)下实验,得到c(NH2COO-)随时间变化关系如图所示.以下分析正确的是( )| A. | 无法判断T1和T2的大小关系 | |
| B. | T1℃时,第6min反应物转化率为6.25% | |
| C. | T2℃时,0~6min ν(NH2COO-)=0.3mol•L-1•min-1 | |
| D. | 往平衡体系加水稀释,平衡右移,溶液中各种离子浓度减小 |
12.一定条件下,下列所发生的反应属于取代反应的是( )
| A. | 天然气的燃烧 | B. | 乙烯使溴水褪色 | ||
| C. | 苯与浓硝酸反应 | D. | 溴乙烷与氢氧化钠的醇溶液反应 |
9.既有离子键,又有共价键的化合物是( )
| A. | KBr | B. | NaOH | C. | HBr | D. | N2 |
16.下列比较中正确的是( )
| A. | 原子半径 Cl>Si>Na | B. | 金属性 Na>Mg>Al | ||
| C. | 碱性 LiOH>NaOH>KOH | D. | 酸性 H3PO4>H2SO4>HClO4 |
13.除去下列杂质(括号中为杂质),采用的试剂和除杂方法错误的是( )
| 选项 | 含杂质的物质 | 试剂 | 除杂方法 |
| A | C2H4(SO2) | 溴水 | 洗气 |
| B | C6H6(Br2) | NaOH溶液 | 分液 |
| C | C6H5NO2(HNO3) | NaOH溶液 | 分液 |
| D | C2H2(H2S) | CuSO4溶液 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
10.若用X、Y、Z和R分别代表四种元素,而且aXm+、bYn+、cZn-、dRm-四种离子的电子层结构都与S2-相同,则下列关系式正确的是( )
| A. | a-b=m-n | B. | b-d=m-n | C. | c-n=18 | D. | a-m=16 |
11.下列有关电子云和原子轨道的说法中正确的是( )
| A. | 原子核外的电子像云雾一样笼罩在原子核周围,故称电子云 | |
| B. | s能级原子轨道呈球形,处于该轨道上的电子只能在球壳内运动 | |
| C. | p能级原子轨道呈哑铃状,随着能层的增加,p能级原子轨道也在增多 | |
| D. | p能级原子轨道与s能级原子轨道的平均半径都随能层序数的增大而增大 |
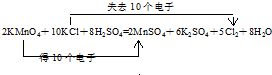 .
.
 ,氯原子核外有17不同运动状态的电子.
,氯原子核外有17不同运动状态的电子.