题目内容
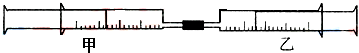
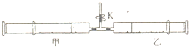 如图所示,将甲.乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(实验均在常温常压下进行).
如图所示,将甲.乙两个装有不同物质的针筒用导管连接起来,将乙针筒内的物质压到甲针筒内,进行下表所列的不同实验(实验均在常温常压下进行).| 实验序号 | 甲针筒内的物质 | 乙针筒内的物质 |
| 1 | 0.3gNa2CO3粉末 | 3mL稀HCl |
| 2 | 0.3gNaHCO3粉末 | 3mL稀HCl |
| 3 | 0.8gNa2O2粉末 | 3ml H2O |
(2)①实验3中的实验现象是:剧烈反应,针筒活塞迅速
②实验3反应后甲针筒内有少量气体,检验该气体的操作及现象是:
操作:打开弹簧夹K,压缩活塞使气体慢慢导出,
③旋转甲.乙两个针筒,使中间导管口朝下,打开弹簧夹K,移动活塞,将实验3针筒中溶液压入滴有酚酞的20mL水中,溶液立即显
分析:(1)碳酸钠与碳酸氢钠都与盐酸反应生成二氧化碳气体,针筒活塞都向外移动;由于碳酸氢钠与盐酸反生成二氧化碳气体的应速率大于碳酸钠,活塞移动速率较快;
(2)①实验3中过氧化钠与水反应生成氧气,针筒内压强增大;温度升高,气体体积增大,根据“反应后将针筒置于空气中使其温度慢慢恢复至常温,发现此过程中针筒活塞慢慢向内移动”可知反应过程中有热量放出;
②根据实验室中常用的检验氧气的方法进行解答;
③过氧化钠与水反应生成氢氧化钠和氧气,反应后的溶液显示碱性,据此进行解答.
(2)①实验3中过氧化钠与水反应生成氧气,针筒内压强增大;温度升高,气体体积增大,根据“反应后将针筒置于空气中使其温度慢慢恢复至常温,发现此过程中针筒活塞慢慢向内移动”可知反应过程中有热量放出;
②根据实验室中常用的检验氧气的方法进行解答;
③过氧化钠与水反应生成氢氧化钠和氧气,反应后的溶液显示碱性,据此进行解答.
解答:(1)由于碳酸钠、碳酸氢钠都与稀盐酸反应生成二氧化碳气体,使针筒中压强增大,活塞向外移动;碳酸氢钠与盐酸反应生成二氧化碳的速率大于碳酸钠的,所以装有碳酸氢钠的针筒活塞移动更快,即活塞移动较快的是实验2,
故答案为:向外;实验2;
(2)①过氧化钠与水反应生成氢氧化钠和氧气,导致针筒中压强增大,针筒向外移动;温度升高,气体体积增大,温度降低,气体体积减小,根据题意“温度慢慢恢复至常温,发现此过程中针筒活塞慢慢向内移动”,说明反应过程中温度升高,该反应为放热反应,反应结束后温度降低,气体体积减小,所以针筒活塞向内移动,
故答案为:向外;放热;
②实验3反应后甲针筒内有少量气体,该气体为氧气,可以使用带火星的小木条进行检验,方法为:将带火星的小木条置于导管口,木条复燃,证明该气体为氧气,
故答案为:将带火星的小木条置于导管口;小木条复燃;
③过氧化钠与水反应的化学方程式为:2Na2O2+2H2O═4NaOH+O2↑,反应中生成氢氧化钠,溶液显示碱性,滴入酚酞溶液显示红色,
故答案为:红;2Na2O2+2H2O═4NaOH+O2↑.
故答案为:向外;实验2;
(2)①过氧化钠与水反应生成氢氧化钠和氧气,导致针筒中压强增大,针筒向外移动;温度升高,气体体积增大,温度降低,气体体积减小,根据题意“温度慢慢恢复至常温,发现此过程中针筒活塞慢慢向内移动”,说明反应过程中温度升高,该反应为放热反应,反应结束后温度降低,气体体积减小,所以针筒活塞向内移动,
故答案为:向外;放热;
②实验3反应后甲针筒内有少量气体,该气体为氧气,可以使用带火星的小木条进行检验,方法为:将带火星的小木条置于导管口,木条复燃,证明该气体为氧气,
故答案为:将带火星的小木条置于导管口;小木条复燃;
③过氧化钠与水反应的化学方程式为:2Na2O2+2H2O═4NaOH+O2↑,反应中生成氢氧化钠,溶液显示碱性,滴入酚酞溶液显示红色,
故答案为:红;2Na2O2+2H2O═4NaOH+O2↑.
点评:本题考查碳酸钠、碳酸氢钠及过氧化钠的性质,题目难度中等,注意掌握常见的钠及其化合物性质,能够正确书写过氧化钠与水、二氧化碳反应的化学方程式,明确具有常见气体的方法.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目