��Ŀ����
�������£���ijһ�ݻ��̶�����������ڳ��붡��(��)��������ʹ�����ڻ��������ѹǿ�ﵽP1�����ȼ�գ����������ǡ�ö���ȫ��Ӧ����ȴ�����º��������������ѹǿΪP2��(���¼�����������λ��Ч����)
(1)������ȼ�յ�������ֻ��H2O(Һ)��CO2���� ��________��
��________��
(2)�� ��0.64����Ӧ�����������������ʵ����ʵ���֮�Ⱥͷ�Ӧǰ������ж�������ʵ���������
��0.64����Ӧ�����������������ʵ����ʵ���֮�Ⱥͷ�Ӧǰ������ж�������ʵ���������
�𰸣�
������
������
|
����(1)0.53 ����(2)������CO2�Ķ�����x mol������CO�Ķ�����y mol���� ����C4H10��6.5O2��4CO2��5H2O(Һ) ����xmol��6.5xmol��4xmol��5xmol ����C4H10��4.5O2��4CO��5H2O(Һ) ����ymol��4.5ymol��4ymol��5ymol ���� ������n(CO2)��n(CO)��n(H2O)��4x��4y��(5x��5y) ������4��0.60y��4y��(5��0.60y��5y)��3��5��10 ���� ������ |

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ
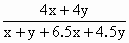 ��0.64�����x��0.6y
��0.64�����x��0.6y ��
��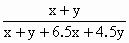
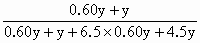 ��0.16
��0.16 ��������������ҡ���������
��������������ҡ���������