题目内容
在某一混合溶液中,含有Na+、Fe3+、Cl-三种离子,其中Na+的质量为46g,Cl-质量为177.5g,问:铁离子的质量为多少g?分析:先根据离子的质量计算出钠离子、氯离子的物质的量,然后根据电荷守恒计算出溶液中铁离子的物质的量,再根据m=nM计算出铁离子的质量.
解答:解:46g钠离子的物质的量为:n(Na+)=
=2mol;
177.5g氯离子的物质的量为:n(Cl-)=
=5mol,
根据电荷守恒可得:n(Na+)+3n(Fe3+)=n(Cl-),n(Fe3+)=
(5mol-2mol)=1mol,
所以溶液中铁离子的质量为:56g/mol×1mol=56g,
答:溶液中铁离子的质量为56g.
| 46g |
| 23g/mol |
177.5g氯离子的物质的量为:n(Cl-)=
| 177.5g |
| 35.5g/mol |
根据电荷守恒可得:n(Na+)+3n(Fe3+)=n(Cl-),n(Fe3+)=
| 1 |
| 3 |
所以溶液中铁离子的质量为:56g/mol×1mol=56g,
答:溶液中铁离子的质量为56g.
点评:本题考查了有关物质的量的简单计算,题目难度中等,注意熟练掌握物质的量与摩尔质量等物理量之间的关系,明确电荷守恒是解答本题的关键.

练习册系列答案
相关题目
下列图示与对应叙述相符合的是( )


| A、图1表示在含等物质的量NaOH、Na2CO3的混合溶液中滴加0.1mol?L-1盐酸至过量时,产生气体的体积与消耗盐酸的关系 | B、图2表示Cl2通入SO2溶液中pH的变化 | C、图3表示10 mL 0.01 mol?L-1KMnO4 酸性溶液与过量的0.1 mol?L-1 H2C2O4溶液混合时,n(Mn2+) 随时间的变化(Mn2+对该反应有催化作用) | D、图4表示已达平衡的某可逆反应,在t0时改变某一条件后反应速率随时间变化,则改变的条件一定是加入催化剂 |

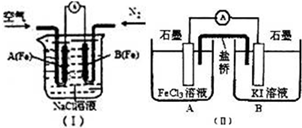 研究铁及铁的化合物的性质具有重要意义.
研究铁及铁的化合物的性质具有重要意义.