题目内容
某体积可变的密闭容器,盛有体积比为2∶3的N2和H2,一定条件下发生反应N2(g)+3H2(g)A.原混合气体的体积为1.2 V B.原混合气体的体积为1.1 V
C.反应中,消耗N2的体积为0.3V D.反应达到平衡时,消耗H2的体积为0.3V
解析:某体积可变的密闭容器,若维持温度和压强不变,则气体的体积之比等于其物质的量之比,依题意可设N2、H2的初始体积分别为2x、3x。
N2(g) + 3H2(g) ![]() 2NH3(g)
2NH3(g)
1 3 2
初始体积: 2x 3x 0
转化体积:![]()
![]() 20%V
20%V
平衡体积:2x-0.1V 3x-0.3V 20%V
2x-0.1V+3x-0.3V+20%V=V
x=![]()
所以原混合气体的体积为:2x+3x=5×![]() =1.2V,A正确,消耗N2的体积为
=1.2V,A正确,消耗N2的体积为![]() =0.1V
=0.1V
达到平衡时,消耗H2的体积为:![]() =0.3V,故D正确。
=0.3V,故D正确。
答案:AD

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
将amol小苏打和bmol过氧化钠置于某体积可变的密闭容器中充分加热,反应后测得容器内的氧气为1mol,下列说法一定正确的是( )
| A、b=2 | B、容器中一定没有残余的CO2和水蒸气 | C、a:b≥1 | D、反应中转移的电子数一定为2NA |
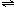 2C若维持温度和压强不变,当达到平衡时,容器的体积为V升,其中C气体的体积占10%,下列推断正确的是( )
2C若维持温度和压强不变,当达到平衡时,容器的体积为V升,其中C气体的体积占10%,下列推断正确的是( )