��Ŀ����
ijУ����С��������ʵ�飺��a mol CO2ͨ��1 L 1 mol��L-1��NaOH��Һ�У�����Һ��ѹ���ɵõ����� m g,������m��a�Ĺ�ϵ��������ȷ��Ϊ�� ���ٵ�0��a��0.5ʱ��m=(26a+40) g �ڵ�0��a��0.5ʱ��m=(26a+40) g �۵�a=0.5ʱ,m=53 g �ܵ�0.5��a��1ʱ�� m=(62a+22) g �ݵ�a��1ʱ��m=106 g��a��1ʱ��m=84 g
A.�٢ڢۢ� B.�ڢۢܢ� C.�ڢܢݢ� D.�٢ۢܢ�
D
������CO2ͨ�뵽NaOH��Һ�п��ܷ����Ļ�ѧ��Ӧ�У�CO2+NaOH====NaHCO3��CO2+2NaOH====NaCO3+H2O��,��ǡ�ð���ʽ��Ӧʱ��a=0.5 mol;��ǡ�ð���ʽ��Ӧʱ��a=1 mol���������ϱ�ʾΪ��
![]()
�����������£���0��a��0.5ʱ������ʽ��Ӧ��CO2�������㣬���õ��Ĺ�������ΪNa2CO3��NaHCO3�Ļ���������Ϊ��m=106 a+(1-2a)��40 g=(26a+40) g,ѡ�����ȷ����a=0.5ʱ�����������ΪNa2CO3,������Ϊ��m=106 a=53 g,��Ӧ��ѡ����ȷ����0.5��a��1ʱ�����������ΪNa2CO3��NaHCO3�Ļ����,��Ӧ���٢�ʽ���У�����������Ϊ��m=106(1-a) g+84(2a-1) g=(62a+22) g,Ӧ��ѡ����ȷ����a��1ʱ������ʽ���з�Ӧ,CO2�й����������õ��Ĺ�������ΪNa2CO3,������Ϊ��m=84 g,��ˣ�ѡ����ȷ������������ȷ��

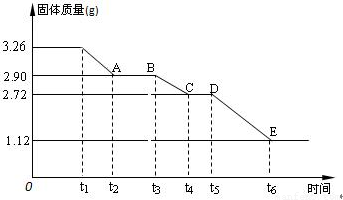
 ijУ����С��Ϊ�ⶨ�Ѳ�����ˮ����ʯ�����ɣ�xCaSO4?yH2O����������ʵ�飺��������ȣ�������ʣ�����������ʱ��仯��ͼ��ʾ������˵��������ǣ�������
ijУ����С��Ϊ�ⶨ�Ѳ�����ˮ����ʯ�����ɣ�xCaSO4?yH2O����������ʵ�飺��������ȣ�������ʣ�����������ʱ��仯��ͼ��ʾ������˵��������ǣ�������| A��t5��t6ʱ��ι������������ԭ���Dz�����SO2��O2�������� | B��t6��õ��Ĺ�����CaSO4 | C��t2��t3ʱ��ι���Ļ�ѧʽΪ2CaSO4?H2O | D��x��y=2��3 |

 �������ʵ�ˮ�����߲ˡ�����Ʒ�ж�����ά����C�������ʳ�֭��ά����C�ĺ�����500 mg��L-1���ҡ�
�������ʵ�ˮ�����߲ˡ�����Ʒ�ж�����ά����C�������ʳ�֭��ά����C�ĺ�����500 mg��L-1���ҡ�