题目内容
18.用CH4和O2组合形成的质子交换膜燃料电池的结构示意图如下: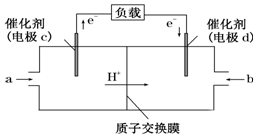
c电极的反应方程式为:CH4-8e-+2H2O═CO2+8H+.
分析 原电池中电子从负极经外电路流向正极,负极反应氧化反应,结合电解质书写电极反应式.
解答 解:因c是电子流出的一极,则c为负极,d为正极,甲烷具有还原性,在负极上发生氧化反应生成CO2,电极反应式为:CH4-8e-+2H2O═CO2+8H+,
故答案为:CH4-8e-+2H2O═CO2+8H+.
点评 本题考查燃料电池电极反应式的书写,难度中等,注意正负极的判断及其电解质溶液的影响.

练习册系列答案
 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
8.下列叙述正确的是( )
| A. | 蛋白质溶液中加入Na2SO4溶液可使其变性 | |
| B. | 氨基酸具有两性,既能与酸反应又能与碱反应 | |
| C. | 蔗糖既能发生水解反应,又能发生银镜反应 | |
| D. | 纤维素在人体内不能水解生成葡萄糖,因此对人体健康无益 |
9.下列说法不正确的是( )
①有化学键被破坏的变化就是化学变化
②用化学键的强弱可以判断氯化钠与溴化钠,氯化氢与溴化氢的熔沸点高低
③质子数相同的微粒不一定是同种元素
④如果ⅡA族某元素原子序数为x,则同周期ⅢA族的元素的原子序数为x+1
⑤如果三周期某元素原子序数为x,则同主族四周期的元素的原子序数为x+8
⑥ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物酸性越强.
①有化学键被破坏的变化就是化学变化
②用化学键的强弱可以判断氯化钠与溴化钠,氯化氢与溴化氢的熔沸点高低
③质子数相同的微粒不一定是同种元素
④如果ⅡA族某元素原子序数为x,则同周期ⅢA族的元素的原子序数为x+1
⑤如果三周期某元素原子序数为x,则同主族四周期的元素的原子序数为x+8
⑥ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物酸性越强.
| A. | ①②④⑤ | B. | ③⑤⑥ | C. | ②④⑥ | D. | ①②④⑤⑥ |
6.下列有关甲烷的说法正确的是( )
| A. | 易溶于水 | B. | 是天然气的主要成分 | ||
| C. | 点燃前不需要验纯 | D. | 与乙烷互为同分异构体 |
10.用蘸有浓氨水的棉棒对输氯管道检漏的原理为:3Cl2+8NH3$?_{高温、高压}^{催化剂}$N2+6NH4Cl.该反应的下列说法正确的是( )
| A. | Cl2被氧化 | |
| B. | NH3得到电子 | |
| C. | Cl2是氧化剂 | |
| D. | 反应每生成1molN2转移电子数约为8×6.02×1023 |
7.下图是乙酸乙酯的合成路线图,下列说法正确的是( )


| A. | 乙醇不能使酸性高锰酸钾溶液褪色 | |
| B. | 物质B的溶液不能与碳酸钙反应 | |
| C. | CH3COOCH2CH3的同分异构体中能与碳酸氢钠溶液反应的有两种 | |
| D. | 反应④属于取代反应 |

 .
. .
. .
. .
. ③
③ ④
④