题目内容
下列说法正确的是( )
| A、120 g NaCl溶液中溶有20 g NaCl,则该温度下NaCl的溶解度为20g |
| B、2 mol/L KCl溶液与1 mol/L K2SO4溶液混合后,c(K+)为2 mol/L |
| C、22.4 L HCl气体溶于水制成1 L溶液,该溶液的物质的量浓度为1 mo1/L |
| D、把5 g胆矾(CuSO4?5H2O)溶于45 g水中,所得溶液溶质的质量分数为10% |
考点:物质的量浓度的相关计算,溶液中溶质的质量分数及相关计算
专题:物质的量浓度和溶解度专题
分析:A.120 g NaCl溶液中溶有20 g NaCl,该溶液不一定是饱和溶液,该温度下NaCl的溶解度不一定为20g;
B.KCl溶液中c(K+)为2 mol/L,K2SO4溶液中c(K+)为2 mol/L,混合后钾离子浓度不变;
C.HCl不一定处于标况下,22.4L HCl的物质的量不一定是1mol;
D.结合化学式计算硫酸铜的质量,再根据
×100%计算硫酸铜的质量分数.
B.KCl溶液中c(K+)为2 mol/L,K2SO4溶液中c(K+)为2 mol/L,混合后钾离子浓度不变;
C.HCl不一定处于标况下,22.4L HCl的物质的量不一定是1mol;
D.结合化学式计算硫酸铜的质量,再根据
| 硫酸铜质量 |
| 溶液质量 |
解答:
解:A.120 g NaCl溶液中溶有20 g NaCl,溶液中水的质量为100g,NaCl质量为20g,该溶液若为饱和溶液,该温度下NaCl的溶解度为20g,若不是饱和溶液,该温度下NaCl的溶解度不是20g,故A错误;
B.KCl溶液中c(K+)为2 mol/L,K2SO4溶液中c(K+)为2 mol/L,混合后溶液中c(K+)为2 mol/L,故B正确;
C.HCl不一定处于标况下,22.4L HCl的物质的量不一定是1mol,溶于水制成1 L溶液,该溶液的物质的量浓度不一定1 mo1/L,故C错误;
D.5g胆矾含有硫酸铜的质量为5g×
=3.2g,溶液中硫酸铜的质量分数为
×100%=6.4%,故D错误,
故选B.
B.KCl溶液中c(K+)为2 mol/L,K2SO4溶液中c(K+)为2 mol/L,混合后溶液中c(K+)为2 mol/L,故B正确;
C.HCl不一定处于标况下,22.4L HCl的物质的量不一定是1mol,溶于水制成1 L溶液,该溶液的物质的量浓度不一定1 mo1/L,故C错误;
D.5g胆矾含有硫酸铜的质量为5g×
| 160 |
| 250 |
| 3.2g |
| 45g+5g |
故选B.
点评:本题考查溶液浓度有关计算,涉及溶解度、质量分数、物质的量浓度,A、C选项为易错点,学生容易忽略溶液是否饱和、气体摩尔体积的使用体积与对象.

练习册系列答案
 精英口算卡系列答案
精英口算卡系列答案 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
在一定条件下,反应N2+3H2?2NH3,在2L密闭容器中进行,5min内氨的物质的量增加了1mol,则有关该反应的速率正确的是( )
| A、υ(H2)=0.15 mol/(L?min) |
| B、υ(N2)=0.2mol/(L?min) |
| C、υ(N2)=0.1 mol/(L?min) |
| D、υ (NH3)=0.2mol/(L?min) |
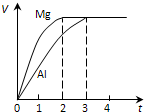 镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图.关于反应中镁和铝的说法正确的是( )
镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如图.关于反应中镁和铝的说法正确的是( )| A、质量之比为3:2 |
| B、物质的量之比为2:3 |
| C、摩尔质量之比为2:3 |
| D、消耗硫酸的物质的量之比为1:1 |
下列有关氧化还原反应的说法正确的是( )
| A、2Na2O2+2H2O=4NaOH+O2↑ 反应中,Na2O2是氧化剂,H2O是还原剂 |
| B、CaH2+2H2O=Ca(OH)2+2H2↑ 反应中,Ca(OH)2既不是氧化产物也不是还原产物 |
| C、KClO3+6HCl=KCl+3Cl2↑+3H2O 反应中,转移的电子数为6e- |
| D、KClO3+6HCl=KCl+3Cl2↑+3H2O 反应中,被氧化的氯元素与被还原的氯元素质量比为6:1 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol S在足量O2中燃烧,转移的电子数为6 NA |
| B、标况下,22.4L氦气含有的原子数为2NA |
| C、28 g C2H4中含有2 NA个碳原子 |
| D、0.1 mol?L-1的碳酸氢钠溶液中含钠离子数为0.1NA |
下列说法不正确的是( )
| A、要想使AlCl3溶液中的Al3+几乎全部沉淀出来,可以加入过量的氨水 |
| B、向FeCl2溶液中加入氨水,最终会看到红褐色沉淀 |
| C、保存硫酸亚铁溶液时常在其中加颗铁钉 |
| D、氢氧化钠、纯碱溶液要存放在带磨砂玻璃塞的试剂瓶中 |
下列物质中,不能导电的电解质是( )
| A、氯酸钾溶液 | B、澄清石灰水 |
| C、酒精 | D、氯化钠晶体 |
下列化学用语正确的是( )
A、H2O2的电子式: | ||
| B、氯气的结构式:Cl-Cl | ||
C、CO2的比例模型: | ||
D、原子核内有20个中子的氯原子:
|