题目内容
把由NaOH、AlCl3、MgCl2三种固体组成的混合物溶于足量水中,有0.58 g白色难溶物析出,向所得溶液中逐滴加入0.5 mol·L-1的盐酸,加入盐酸的体积和生成沉淀的质量如图所示: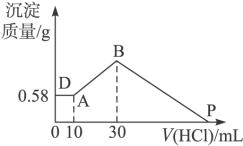
(1)混合物中NaOH的质量是___________g,AlCl3的质量是___________g,MgCl2的质量为___________g。
(2)P点表示盐酸加入的体积为___________mL。
(1)2.6 1.335 0.95 (2)130 解析:(1)由图可知,三种物质混合时有0.58 g沉淀,当向此混合物中加入10 mL盐酸时,沉淀质量不变,说明混合物中NaOH过量,该沉淀是Mg(OH)2,由镁元素守恒可知:n(MgCl2)=n〔Mg(OH)2〕= 2NaOH—MgCl2—Mg(OH)2 0.02 mol 0.01 mol AlCl3 — NaAlO2—HCl 0.01 mol m(AlCl3)=0.01 mol×133.5 g·mol-1=1.335 g 由图可知,B点是沉淀量最大点,此时溶液中溶质只有NaCl,由元素守恒可知: n(NaOH)=n(HCl)+2n(MgCl2)+3n(AlCl3)=0.5 mol·L-1×0.03 L+2×0.01 mol+3×0.01 mol=0.065 mol,所以,m(NaOH)=0.065 mol×40 g·mol-1=2.6 g。 (2)由图可知,P点时Al(OH)3、Mg(OH)2沉淀恰好全部溶解在盐酸中,溶质为NaCl、AlCl3、MgCl2,所以,此时溶解Al(OH)3、Mg(OH)2沉淀恰好消耗盐酸: V(HCl)= 由此可知,P点时,V(HCl)=30 mL+100 mL=130 mL。![]() =0.01 mol,故m(MgCl2)=0.01 mol×95 g·mol-1=0.95 g。由以下关系得:
=0.01 mol,故m(MgCl2)=0.01 mol×95 g·mol-1=0.95 g。由以下关系得:![]() ×0.5 mol·L-1=0.01 mol
×0.5 mol·L-1=0.01 mol![]() =0.1 L=100 mL。
=0.1 L=100 mL。

1加1阅读好卷系列答案
专项复习训练系列答案
初中语文教与学阅读系列答案

完形填空与阅读理解周秘计划系列答案
英语阅读理解150篇系列答案
奔腾英语系列答案
标准阅读系列答案
53English系列答案
考纲强化阅读系列答案
 把由NaOH、AlCl3与MgCl2三种固体组成的混合物溶于足量水中,有2.9g白色沉淀析出,向所得的浊液里逐滴加入2mol?L-1的盐酸,加入盐酸的体积和生成沉淀的质量关系如图所示.试判断p点所表示的加入盐酸的体积是( )
把由NaOH、AlCl3与MgCl2三种固体组成的混合物溶于足量水中,有2.9g白色沉淀析出,向所得的浊液里逐滴加入2mol?L-1的盐酸,加入盐酸的体积和生成沉淀的质量关系如图所示.试判断p点所表示的加入盐酸的体积是( )| A、135 mL | B、145 mL | C、155 mL | D、165 mL |
 Ⅰ把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中,有0.58g白色沉淀析出,向所得浊液中,逐滴加入1mol/L盐酸,加入盐酸的体积和生成沉淀的质量如图所示.
Ⅰ把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中,有0.58g白色沉淀析出,向所得浊液中,逐滴加入1mol/L盐酸,加入盐酸的体积和生成沉淀的质量如图所示.

