��Ŀ����
(12��) ������AX3�͵���X2��һ�������·�Ӧ�����ɻ�����AX5���ش��������⣺
��ӦAX3(g)��X2(g) AX5(g)���ݻ�Ϊ10 L���ܱ������н��С���ʼʱAX3��X2��Ϊ0.2 mol����Ӧ�ڲ�ͬ�����½��У���Ӧ��ϵ��ѹǿ��ʱ��ı仯��ͼ��ʾ��
AX5(g)���ݻ�Ϊ10 L���ܱ������н��С���ʼʱAX3��X2��Ϊ0.2 mol����Ӧ�ڲ�ͬ�����½��У���Ӧ��ϵ��ѹǿ��ʱ��ı仯��ͼ��ʾ��

����ʽ����ʵ��a�ӷ�Ӧ��ʼ���ﵽƽ��ʱ�ķ�Ӧ���� v(AX3)�� ��
��ͼ��3��ʵ��ӷ�Ӧ��ʼ���ﵽƽ��ʱ�ķ�Ӧ����v(AX5)��С����Ĵ���Ϊ (��ʵ�����)��
����ʵ��a��ȣ���������ı��ʵ���������ж������ǣ�
b ��
c�� ��
����p0��ʾ��ʼʱ��ѹǿ��p��ʾƽ��ʱ��ѹǿ������ʾAX3��ƽ��ת���ʣ�����ı���ʽΪ ��
(10��) (ÿ��2��)
1.7��10-4mol/��L?min����2�֣�
�� acb ��2�֣�
�ۼ����������Ӧ���ʼӿ죬��ƽ���û�иı� ��2�֣���
�¶����ߡ���Ӧ���ʼӿ죬��ƽ������淴Ӧ�����ƶ�����Ӧ�������ݻ�����ʼ���ʵ���δ�ı䣬����ʼ��ѹǿ����2�֣���
�ܦ�=2��1- ����2�֣���
����2�֣���
��������
����������ٷ�Ӧ����=��λʱ���ڵ����ʵ�Ũ�ȵĸı�������ͼ���֪��ƽ��ʱʵ��a�е�ѹǿ��ԭ����160��Ϊ120kPa��˵����������ʵ�������Ϊԭ����120/160=3/4, ��AX3�����ʵ�������x,����
AX3(g)��X2(g) AX5(g)
AX5(g)
��ʼ��mol�� 0.2 0.2 0
ת����mol�� x x x
ƽ�⣨mol�� 0.2-x 0.2-x x
����0.2-x+0.2-x+x=3/4(0.2+0.2),���x=0.1mol������ƽ���ʱ����60min����Ӧ���� v(AX3)��0.1mol/10L/60min=1.7��10-4mol/��L?min����
�ڸ��ݵ���ƽ�����õ�ʱ��Ķ����жϷ�Ӧ���ʵĿ���������ʱ��Խ�̣���Ӧ����Խ�죬��ͼ��֪�ﵽƽ��ʱ�ķ�Ӧ����v(AX5)��С����Ĵ���Ϊacb��
��b��a�ﵽ��ƽ����ͬ������Ӧ���ʿ죬˵��bʹ���˴�������c�ķ�Ӧ���ʱ�a�죬˵��c���¶�����ѹǿ�������Ǻ��ߣ�ѹǿ����ƽ�������ƶ���ѹǿ���ٵĸ��࣬����Ӧ��b���·�����ͼ��������ֻ���������¶ȣ�ʹƽ�������ƶ���ѹǿ���ٵĽ�a�٣�
����p0��ʾ��ʼʱ��ѹǿ��p��ʾƽ��ʱ��ѹǿ������ʾAX3��ƽ��ת���ʣ���AX3�����ʵ�������x�����ݢٵļ�����̿�֪����0.4-x��/0.4=p/ p0,���x=0.4��p0-p��/p0�����=0.4��p0-p��/p0/0.2=2��1- ��.
��.
���㣺���黯ѧ��Ӧ���ʡ���ѧƽ��ļ��㣬ƽ��ͼ����ж�

25 ��ʱ������ƽ�ⳣ����
��ѧʽ | CH3COOH | H2CO3 | HClO |
����ƽ�ⳣ�� | 1.8��10��5 | K1 4.3��10��7 K2 5.6��10��11 | 3.0��10��8 |
�ش��������⣺
��1�����ʵ���Ũ��Ϊ0.1 mol/L�������������ʣ�a.Na2CO3��b.NaClO��c.CH3COONa��d.NaHCO3��pH�ɴ�С��˳����________________��(����)
��2��������0.1 mol/L��CH3COOH��Һ��ˮϡ���̣����б���ʽ������һ����С����_____��
A��c(H��) B��c(H��)/c(CH3COOH) C��c(H��)��c(OH��) D��c(OH��)/c(H��)
��3�����Ϊ10 mL pH��2�Ĵ�����Һ��һԪ��HX�ֱ��ˮϡ����1 000 mL��ϡ����pH�仯��ͼ����HX�ĵ���ƽ�ⳣ��________(����ڡ��������ڡ���С�ڡ�)�����ƽ�ⳣ����������__________________��

ϡ�ͺ�HX��Һ��ˮ���������c(H��)________������Һ��ˮ���������c(H��)(����ڡ��������ڡ���С�ڡ�)�������ǣ�__________________��
��4��25 ��ʱ��CH3COOH��CH3COONa�Ļ����Һ������û��ҺpH��6������Һ��c(CH3COO��)��c(Na��)��________��(��ȷ��ֵ)
( I) ��һ���ݻ��̶�������ܱ������н��з�Ӧ��
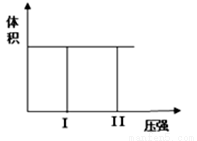
2X(g) + Y(g)  2Z(g) ����2molX��1molY���������ʱ������״ ̬I�� ��Ӧ�ھ��������´ﵽƽ��ʱ����״̬II������ͼ������÷�Ӧ�ġ�H 0; ( ���< ��> �� = ��)���÷�Ӧ�� ����:���»���£����������Է����С�
2Z(g) ����2molX��1molY���������ʱ������״ ̬I�� ��Ӧ�ھ��������´ﵽƽ��ʱ����״̬II������ͼ������÷�Ӧ�ġ�H 0; ( ���< ��> �� = ��)���÷�Ӧ�� ����:���»���£����������Է����С�
(II)���ݻ��ɱ���ܱ������з�����Ӧ��mA(g) + nB(g)  pC(g) ,
pC(g) ,
��һ���¶ȺͲ�ͬѹǿ�´ﵽƽ��ʱ���ֱ�õ�A�����ʵ���Ũ����
�±�
ѹǿp/Pa | 2��105 | 5��105 | 1��106 |
c(A)/mol��L-1 | 0.08 | 0.20 | 0.44 |
��1����ѹǿ��2��105 Pa���ӵ�5��105 Paʱ��ƽ�� �ƶ�������� ���� ������
��2��ά��ѹǿΪ2��105 Pa������Ӧ�ﵽƽ��״̬ʱ����ϵ�й���amol���壬������ϵ�м���bmolB,�����´ﵽƽ��ʱ����ϵ�����������ʵ����� mol.
��3����ѹǿΪ1��106 Paʱ���˷�Ӧ��ƽ�ⳣ������ʽ�� ��
��4������������ͬʱ������������ѹǿ�·ֱ����÷�Ӧ��2��105 Paʱ��
A��ת������ʱ��仯����ͼ������ͼ�в��仭��ѹǿ�ֱ�Ϊ5��105 Pa
��1��106 Paʱ��A��ת������ʱ��ı仯���ߣ�����ͼ���ϱ��ѹǿ����

������ʵ������ƽ���ƶ�ԭ�����͵��ǣ� ��
2SO2+O2 ��ƽ����ϵ�У�������18O���ɵ���������SO2�е�18O�ĺ��������� |
|
|
| ||||||||||||
A | B | C | D |
�����й���֮���ϵ������������ȷ���ǣ� ����
ѡ�� | �� | ���ϵ | �������� |
A | C60��C70��C540 | ͬλ�� | ����ֻ���Ǽ��Թ��ۼ� |
B | �����顢2��2-�������� | ͬ���칹�� | ���³�ѹ�³���̬ |
C | ͬ�������� | ������������ʱ�Ĵ��� | |
D | ���ᡢӲ֬�� | ͬϵ�� | �ܷ���������Ӧ |
 Al(OH)3
Al(OH)3
 2SO3
2SO3