题目内容
(1)阿波罗宇宙飞船使用的是氢氧燃料电池,其电极反应为:
2H2+4OH――4e-=4H2O,O2+2H2O+4e-=4OH-。正极发生的是 反应(填氧化或还原),总反应方程式是 。
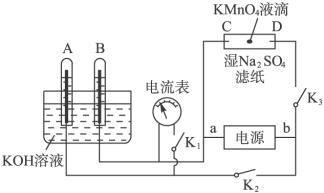
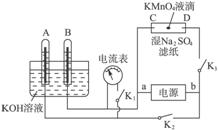
(2)如图装置,A、B中的电极为多孔的惰性电极;C、D为夹在湿的Na2SO4滤纸条中心
的铂夹;电源有a、b两极。若在A、B中充满KOH溶液后倒立于KOH溶液的水槽中。切断K1,闭合K2、K3通直流电,则:
①标出电源的正、负极,a为 极,b为 极。
②在湿的Na2SO4溶液滤纸条中心的KMnO4液滴,有什么现象 。
③写出电极反应式:A中 。B中 。
④若电解一段时间后,A、B中均有气体包围电极。此时切断K2、K3,闭合K1,则电流表的指针是否移动(填是或否) 。
⑤若电流表指针不移动说明理由,若指针移动也说明理由。
。
解析:
(1)还原;2H2+O2=2H2O; (2)①负;正; ②紫色液滴向D移动; ③A:4OH――4e-=2H2O+O2↑;B:4H++4e-=2H2↑; ④是; ⑤形成氢氧燃料电池
|
提示:
(1)氢氧燃料电池是用KOH溶液作电解质,氢气和氧气分别在两极发生反应,将化学能转化为电能的装置。由于失去电子的一极为负极,所以氢气在负极发生反应,失电子化合价升高被氧化,发生氧化反应;得到电子的一极为正极,氧气在正极发生反应,得电子被还原,发生还原反应。 (2)①电解KOH溶液实际就是电解水,所得产物为H2和O2,因为B试管中气体体积是A试管的2倍,所以B中为H2,A中为O2,即B为阴极,A为阳极,所以a为负极,b为正极。 ②当切断K1,闭合K2、K3,通直流电时,实际形成了以硫酸钠溶液作电解质的电解池。在外电场的作用下,紫色的MnO ③A、B两极发生的电极反应,即为(1)中的反应。 ④⑤如果切断K2、K3,闭合K1,则可由B中的H2,A中的O2与KOH溶液形成H2-O2燃料电池,把化学能变为电能,故指针偏转。
|

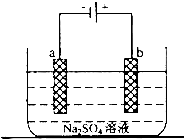 (1)阿波罗宇宙飞船使用的是碱性氢氧燃料电池,负极贮存的是氢气,正极贮存的是氧气,电解质是NaOH溶液.请写出该反应发生的电极反应式.
(1)阿波罗宇宙飞船使用的是碱性氢氧燃料电池,负极贮存的是氢气,正极贮存的是氧气,电解质是NaOH溶液.请写出该反应发生的电极反应式.