题目内容
对于a mol H2O和a mol CO2的说法正确的是( )
分析:A、相同条件下,气体的物质的量相同,体积相同;
B、密度是用质量除以体积得到;
C、物质的量相同,分子数相同;
D、物质的量和摩尔质量可以求得质量;
B、密度是用质量除以体积得到;
C、物质的量相同,分子数相同;
D、物质的量和摩尔质量可以求得质量;
解答:解:A、相同条件下a molH2O和a molCO2,必须都是气态状况下体积才相同,故A错误;
B、相同条件下,密度用质量除以体积,但相同条件下水的状态可以是水,也可以是气态,a molH2O和a molCO2的质量不同,体积也可能不同,所以密度不一定相同,故B错误;
C、a molH2O和a molCO2,根据物质的量意义所含水分子数和二氧化碳分子数相同,原子数也相同,故C正确;
D、质量比为(a mol×18g?mol-1):(a mol×44g?mol-1)=9:22,故D错误;
故选C.
B、相同条件下,密度用质量除以体积,但相同条件下水的状态可以是水,也可以是气态,a molH2O和a molCO2的质量不同,体积也可能不同,所以密度不一定相同,故B错误;
C、a molH2O和a molCO2,根据物质的量意义所含水分子数和二氧化碳分子数相同,原子数也相同,故C正确;
D、质量比为(a mol×18g?mol-1):(a mol×44g?mol-1)=9:22,故D错误;
故选C.
点评:本题考查了阿伏伽德罗定律的应用,物质的量、密度的有关计算.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
哥本哈根会议虽未能就减排问题达成有约束力的协议,但各国对于CO2对气候的影响达成了共识,都在积极研究方法循环利用CO2.CO2(g)与H2(g)反应可生成CH3OH(g)和H2O(g).某实验小组为研究该反应进行了如下实验.在某温度下,向容积为10L的恒温恒容容器中充入a mol CO2和a mol H2,测得不同时刻的c(H2)如右表.
(1)写出生成CH3OH反应的化学方程式: .若达平衡状态时,放出的热量为58.8kJ,则上述反应的△H= .0~10min内,CH3OH的平均反应速率v(CH3OH)= .
(2)下列措施能使平衡体系中 增大的是 (填字母).
增大的是 (填字母).
A、升高温度 B、充入Ar使压强增大
C、再充入0.5a mol CO2和0.5a mol H2D、将水从平衡体系中分离出来
(3)a= ,该温度下上述反应的平衡常数K= (精确到0.1).
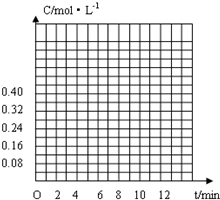
(4)在如图所示的坐标系中,画出CO2和H2的浓度随时间变化的图象.

| 时间/min | C(H2)/mol.L-1 |
| 0.40 | |
| 2 | 0.28 |
| 4 | 0.19 |
| 6 | 0.13 |
| 8 | 0.08 |
| 10 | 0.04 |
| 12 | 0.04 |
(2)下列措施能使平衡体系中
 增大的是 (填字母).
增大的是 (填字母).A、升高温度 B、充入Ar使压强增大
C、再充入0.5a mol CO2和0.5a mol H2D、将水从平衡体系中分离出来
(3)a= ,该温度下上述反应的平衡常数K= (精确到0.1).
(4)在如图所示的坐标系中,画出CO2和H2的浓度随时间变化的图象.

 化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料. 哥本哈根会议虽未能就减排问题达成有约束力的协议,但各国对于CO2对气候的影响达成了共识,都在积极研究方法循环利用CO2.CO2(g)与H2(g)反应可生成CH3OH(g)和H2O(g).某实验小组为研究该反应进行了如下实验.在某温度下,向容积为10L的恒温恒容容器中充入a mol CO2和a mol H2,测得不同时刻的c(H2)如右表.
哥本哈根会议虽未能就减排问题达成有约束力的协议,但各国对于CO2对气候的影响达成了共识,都在积极研究方法循环利用CO2.CO2(g)与H2(g)反应可生成CH3OH(g)和H2O(g).某实验小组为研究该反应进行了如下实验.在某温度下,向容积为10L的恒温恒容容器中充入a mol CO2和a mol H2,测得不同时刻的c(H2)如右表. CH3OH+H2O
CH3OH+H2O