题目内容
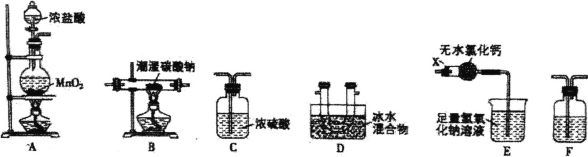
【题目】现用Na2SO4固体来配制480mL0.2mol·L-1的Na2SO4溶液。可供选择的仪器如图:
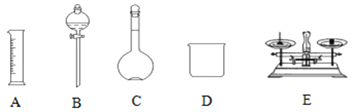
(1)如图所示的仪器中配制溶液不需要的是__ (填选项),配制上述溶液还需用到的玻璃仪器是___、__ (填仪器名称)。
(2)使用容量瓶之前必须进行的操作是___。(填选项)
A.检查气密性 B.检查是否漏水 C.烘干
(3)经计算,需Na2SO4的质量为___g。
(4)你选用的容量瓶规格为___mL。
(5)配制溶液时,一般可分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容
其操作顺序:②→__→__→__→__→__→__(填序号)。___
(6)在配制过程中,其他操作都准确,定容时俯视刻度线会使所配溶液浓度__(填“偏高”、“偏低”或“无影响”)。
【答案】B 胶头滴管 玻璃棒 B 14.2 500 ①③⑤⑥⑦④ 偏高
【解析】
(1)根据配制一定物质的量浓度溶液的操作步骤选取实验仪器;
(2)容量瓶带有瓶塞,为防止使用过程中漏水,使用前应检查是否漏液;
(3)依据m=cVM计算;
(4)根据实验室常见容量瓶的规格选择;
(5)根据配制一定物质的量浓度溶液的操作步骤排序;
(6)定容时俯视刻度线,会导致溶液的体积偏小,据此分析判断。
(1)配制一定物质的量浓度的溶液的步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称取硫酸钠,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以需要的仪器有托盘天平、玻璃棒、量筒、胶头滴管、小烧杯、500mL容量瓶,所以用不到的仪器有分液漏斗,还缺少的仪器:胶头滴管、玻璃棒,故答案为:B;胶头滴管;玻璃棒;
(2)容量瓶带有瓶塞,为防止使用过程中漏水,使用前应检查是否漏液,故答案为:B;
(3)实验室没有480mL的容量瓶,应该选用500 mL的容量瓶配制,Na2SO4的质量为0.5L×0.2mol/L×142g/mol=14.2g,故答案为:14.2;
(4)实验室没有480mL的容量瓶,应该选用500 mL的容量瓶配制,故答案为:500;
(5)配制一定物质的量浓度的溶液的步骤有计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等操作,所以正确的操作顺序为②①③⑤⑥⑦④,故答案为:①③⑤⑥⑦④;
(6)在配制过程中,其他操作都准确,定容时俯视刻度线,导致溶液的体积偏小,会使所配溶液浓度偏高,故答案为:偏高。

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案