��Ŀ����
�������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӡ�
 ��Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬�����Ϊ1 L���ܱ������У�����1mol CO2��3mol H2��һ�������·�����Ӧ��
��Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬�����Ϊ1 L���ܱ������У�����1mol CO2��3mol H2��һ�������·�����Ӧ��
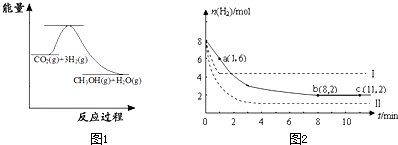
CO2(g)��3H2(g)![]() CH3OH(g)��H2O(g) ��H����49.0kJ/mol
CH3OH(g)��H2O(g) ��H����49.0kJ/mol
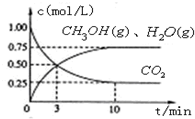
���CO2��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ��
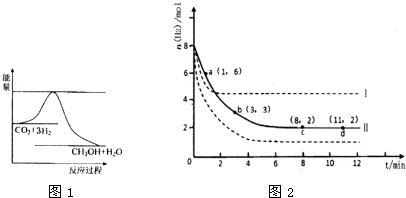
�ٴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v(H2)��___________mol/(L��min)��
�ڸ÷�Ӧ��ƽ�ⳣ������ʽΪ__________________��
�����д�ʩ����ʹn(CH3OH)��n(CO2)�������___________��
A�������¶� B������He(g)��ʹ��ϵѹǿ����
C����H2O(g)����ϵ�з��� D���ٳ���1mol CO2��3mol H2
�������˺���������̬ϵͳ�У�����Ҫ�����ȥ��CO2����Ҫ���ṩ�����O2��ij�ֵ绯ѧװ�ÿ�ʵ������ת����2 CO2��2 CO��O2��CO������ȼ�ϡ�
��֪�÷�Ӧ��������ӦΪ��4OH�D�D4e�D��O2����2H2O
��������ӦʽΪ��________________________________��
���������������Ʒ�Ӧ2CO��2C��O2����H��0����S��0��������CO����Ⱦ�������ж��Ƿ���в�˵�����ɣ�______________________________________________��
����0.225 �� ��C��D
��2CO2��4e�D��2H2O��2 CO��4OH�D �������У��÷�Ӧ��һ���������ؼ��ķ�Ӧ���κ�����²����Է�����
����:
(1) �� ������֪v(H2)����C (H2)/��t=2.25 mol��L-1/10min=0.225 mol��L-1��min-1
�� ��ƽ�ⳣ������ʽֱ���Ƴ�����ʽ���ɡ�
�� n(CH3OH)��n(CO2)����ƽ�������ƶ���Ӧ����ɳ����ԭ����֪�𰸡� B��һ���Ի��ԣ���Ϊ����������䣬�交����Ȼ��ѹǿ����������Ũ��δ�����仯����ƽ�ⲻ�ƶ���
��2�����ܷ�Ӧʽ��ȥ������Ӧʽ���ɵ�������Ӧʽ��
2 CO2 ��4OH�D+4e�D �� 2 CO ��2H2O �� 2 CO2 + 2H2O +4e�D �� 2 CO +4OH�D


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�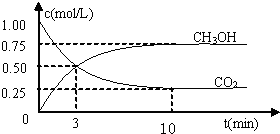 �������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ��ע
�������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ��ע