题目内容
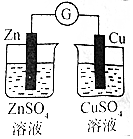
7. 如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液.回答下列问题:
如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液.回答下列问题:银电极上发生还原 反应(“氧化”或“还原”),电极反应式为Cu2++2e-=Cu,该原电池的总反应离子方程式为Zn+Cu2+=Zn2++Cu.
分析 由图可知,Zn为负极,失去电子,Ag为正极,正极上铜离子得到电子,以此来解答.
解答 解:银锌原电池以硫酸铜为电解质溶液,Ag为正极,铜离子得到电子发生还原反应,电极反应为Cu2++2e-=Cu,负极上Zn失去电子,电池总离子反应为Zn+Cu2+=Zn2++Cu,
故答案为:还原;Cu2++2e-=Cu;Zn+Cu2+=Zn2++Cu.
点评 本题考查原电池,为高频考点,把握电极、电极反应、工作原理为解答的关键,侧重分析与应用能力的考查,注意原电池与氧化还原反应的联系,题目难度不大.

练习册系列答案
相关题目
2. 把一块镁铝合金投入到1mol/L 盐酸里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如下图所示.下列说法中不正确的是( )
把一块镁铝合金投入到1mol/L 盐酸里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如下图所示.下列说法中不正确的是( )
 把一块镁铝合金投入到1mol/L 盐酸里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如下图所示.下列说法中不正确的是( )
把一块镁铝合金投入到1mol/L 盐酸里,待合金完全溶解后,往溶液里加入1mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如下图所示.下列说法中不正确的是( )| A. | 生成Al(OH)3沉淀的最大质量为0.78g | B. | 加入70ml NaOH 时溶液呈碱性 | ||
| C. | $\frac{n(Mg)}{n(Al)}$的最大值为1.5 | D. | a的取值范围为0≤a<45mL |
12.在反应A(g)+2B(g)═3C(g)+4D(g)中,表示该反应速率最快的是( )
| A. | v(A)=0.2 mol/(L•s) | B. | v(B)=0.6 mol/(L•s) | C. | v(C)=0.8 mol/(L•s) | D. | v(D)=1 mol/(L•s) |
16.根据元素周期表和元素周期律,判断下列叙述正确的是( )
| A. | 单质氧化性:I2>Br2>Cl2 | B. | 碱性强弱:KOH>NaOH>Mg(OH)2 | ||
| C. | 酸性强弱:HIO4>HBrO4>HClO4 | D. | 热稳定性:PH3>H2S>HCl |
14.下列事实,不能用氢键知识解释的是( )
| A. | 水比硫化氢稳定 | B. | 水和乙醇可以完全互溶 | ||
| C. | 冰的密度比液态水的密度小 | D. | 氟化氢的沸点高于氯化氢 |

 、SO42-
、SO42-