题目内容
碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液,生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g)△H1(1)其他条件相同,CH3OCOOCH3的平衡转化率(α)与温度(T)、反应物配比(R)的关系如图所示.
①△H1______0(填“<”、“=”或“>”).
②由图可知,为了提高CH3OCOOCH3的平衡转化率,除了升温,另一措施是______.
③在密闭容器中,将1mol C2H5OCOOC2H5和1mol CH3OCOOCH3混合加热到650K,利用图中的数据,求此温度下该反应的平衡常数K=______.
(2)已知上述反应需要催化剂,请在答题卡的坐标图中,画出有催化剂与无催化剂两种情况下反应过程中体系能量变化示意图,并进行必要标注.
(3)已知CH3OCOOCH3(g)+C2H5OH(g)?CH3OCOOC2H5(g)+CH3OH(g)△H2
CH3OCOOC2H5(g)+C2H5OH(g)?C2H5OCOOC2H5(g)+CH3OH(g)△H3
△H1=______(用△H2和△H3表示)

【答案】分析:(1)①由图可知,温度越大,CH3OCOOCH3的平衡转化率越大;
②由图可知,温度越大,R越大,CH3OCOOCH3的平衡转化率越大;
③由图可知,R=1,650K,CH3OCOOCH3的平衡转化率为60%,则
C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g)
开始
 0
0
平衡


K为平衡时生成物浓度幂之积与反应物浓度幂之积的比;
(2)催化剂不影响反应热,但催化剂降低反应所需的活化能,以此来图画;
(3)已知②CH3OCOOCH3(g)+C2H5OH(g)?CH3OCOOC2H5(g)+CH3OH(g)△H2,
③CH3OCOOC2H5(g)+C2H5OH(g)?C2H5OCOOC2H5(g)+CH3OH(g)△H3,
根据盖斯定律可知,②-③可得C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g).
解答:解:(1)①由图可知,温度越大,CH3OCOOCH3的平衡转化率越大,则该反应的正反应为吸热反应,所以△H>0,故答案为:>;
②由图可知,温度越大,R越大,CH3OCOOCH3的平衡转化率越大,则除升温外,还可增大反应物中C2H5OCOOC2H5的浓度(或比例),故答案为:增大反应物中C2H5OCOOC2H5的浓度(或比例);
③由图可知,R=1,650K,CH3OCOOCH3的平衡转化率为60%,设容器的体积为VL,则
C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g)
开始
 0
0
平衡


K= =9,故答案为:9;
=9,故答案为:9;
(2)催化剂不影响反应热,但催化剂降低反应所需的活化能,如图所示催化剂对反应的影响为 ,
,
故答案为: ;
;
(3)已知②CH3OCOOCH3(g)+C2H5OH(g)?CH3OCOOC2H5(g)+CH3OH(g)△H2,
③CH3OCOOC2H5(g)+C2H5OH(g)?C2H5OCOOC2H5(g)+CH3OH(g)△H3,
根据盖斯定律可知,②-③可得C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g),则△H1=△H2,-△H3,
故答案为:△H2,-△H3.
点评:本题考查化学平衡的影响因素及化学平衡的计算,反应热的计算,注意学生能力的考查,明确图象的分析是解答的关键,注意催化剂不能改变反应热,题目难度中等.
②由图可知,温度越大,R越大,CH3OCOOCH3的平衡转化率越大;
③由图可知,R=1,650K,CH3OCOOCH3的平衡转化率为60%,则
C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g)
开始

 0
0平衡



K为平衡时生成物浓度幂之积与反应物浓度幂之积的比;
(2)催化剂不影响反应热,但催化剂降低反应所需的活化能,以此来图画;
(3)已知②CH3OCOOCH3(g)+C2H5OH(g)?CH3OCOOC2H5(g)+CH3OH(g)△H2,
③CH3OCOOC2H5(g)+C2H5OH(g)?C2H5OCOOC2H5(g)+CH3OH(g)△H3,
根据盖斯定律可知,②-③可得C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g).
解答:解:(1)①由图可知,温度越大,CH3OCOOCH3的平衡转化率越大,则该反应的正反应为吸热反应,所以△H>0,故答案为:>;
②由图可知,温度越大,R越大,CH3OCOOCH3的平衡转化率越大,则除升温外,还可增大反应物中C2H5OCOOC2H5的浓度(或比例),故答案为:增大反应物中C2H5OCOOC2H5的浓度(或比例);
③由图可知,R=1,650K,CH3OCOOCH3的平衡转化率为60%,设容器的体积为VL,则
C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g)
开始

 0
0平衡



K=
 =9,故答案为:9;
=9,故答案为:9;(2)催化剂不影响反应热,但催化剂降低反应所需的活化能,如图所示催化剂对反应的影响为
 ,
,故答案为:
 ;
;(3)已知②CH3OCOOCH3(g)+C2H5OH(g)?CH3OCOOC2H5(g)+CH3OH(g)△H2,
③CH3OCOOC2H5(g)+C2H5OH(g)?C2H5OCOOC2H5(g)+CH3OH(g)△H3,
根据盖斯定律可知,②-③可得C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g),则△H1=△H2,-△H3,
故答案为:△H2,-△H3.
点评:本题考查化学平衡的影响因素及化学平衡的计算,反应热的计算,注意学生能力的考查,明确图象的分析是解答的关键,注意催化剂不能改变反应热,题目难度中等.

练习册系列答案
相关题目
 碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液.生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g).其他条件相同,CH3OCOOCH3的平衡转化率(α)与温度(T)、反应物配比( R=n(C2H3OCOOC2H5):n(CH3OCOOCH3 )的关系如图所示.三种反应物配比分别为1:1、2:1、3:1.下列说法不正确的是.( )
碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液.生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g).其他条件相同,CH3OCOOCH3的平衡转化率(α)与温度(T)、反应物配比( R=n(C2H3OCOOC2H5):n(CH3OCOOCH3 )的关系如图所示.三种反应物配比分别为1:1、2:1、3:1.下列说法不正确的是.( )| A、该反应△H>0 | B、R1对应的反应物配比为3:1 | C、650℃,反应物配比为1:1时,平衡常数K=6 | D、当C2H5OCOOC2H5与CH3OCOOC2H5生成速率比为1:2时,反应达到平衡状态 |
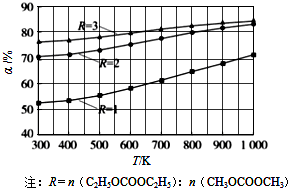 (2012?广州一模)碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液,生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g)△H1
(2012?广州一模)碳酸甲乙酯(CH3OCOOC2H5)是一种理想的锂电池有机电解液,生成碳酸甲乙酯的原理为:C2H5OCOOC2H5(g)+CH3OCOOCH3(g)?2CH3OCOOC2H5(g)△H1 (2013?东城区二模)已知:
(2013?东城区二模)已知: 是碳酸甲乙酯的工业生产原理.如图是投料比[
是碳酸甲乙酯的工业生产原理.如图是投料比[ ]分别为3:1和1:1、反应物的总物质的量相同时,
]分别为3:1和1:1、反应物的总物质的量相同时, 的平衡转化率与温度的关系曲线.下列说法正确的是( )
的平衡转化率与温度的关系曲线.下列说法正确的是( ) 2
CH3OCOOC2H5(g).其他条件相同,CH3OCOOCH3的平衡转化率(α)与温度(T),反应物配比(R=n(C2H5OCOOC2H5):n(CH3OCOOCH3))的关系如下图所示. 三种反应物配比分别为1:1,2:1,3:1.下列说法不正确的是( )
2
CH3OCOOC2H5(g).其他条件相同,CH3OCOOCH3的平衡转化率(α)与温度(T),反应物配比(R=n(C2H5OCOOC2H5):n(CH3OCOOCH3))的关系如下图所示. 三种反应物配比分别为1:1,2:1,3:1.下列说法不正确的是( )
 是碳酸甲乙酯的工业生产原理。下图是投料比[
是碳酸甲乙酯的工业生产原理。下图是投料比[ ]分别为3︰1和1︰1、反应物的总物质的量相同时,
]分别为3︰1和1︰1、反应物的总物质的量相同时, 的平衡转化率与温度的关系曲线。下列说法正确的是
的平衡转化率与温度的关系曲线。下列说法正确的是