题目内容
【题目】水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在100℃时,pH=6,该温度下0.1molL-1的NaOH溶液中,溶液的pH= .
(2)25℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为 , 由水电离出的c(OH-)= mol·L-1.
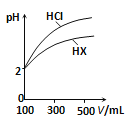
(3)体积均为100mL、pH均为2的盐酸与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX是 (填“强酸”或“弱酸”),理由是 .
【答案】(1)11;
(2)CO32-+H2O![]() HCO3-+OH-;HCO3-+H2O
HCO3-+OH-;HCO3-+H2O![]() H2CO3+OH-;10-3
H2CO3+OH-;10-3
(3)弱酸;稀释相同倍数
【解析】
试题分析:(1)纯水在100 ℃时,pH=6,这说明该温度下水的离子积常数是10-12,因此该温度下0.1 mol·L-1的NaOH溶液中,氢离子浓度是10-11mol/L,则溶液的pH=11。
(2)25 ℃时,向水中加入少量碳酸钠固体,碳酸根水解,得到pH为11的溶液,则其水解的离子方程式为CO32-+H2O![]() HCO3-+OH-;HCO3-+ H2O
HCO3-+OH-;HCO3-+ H2O ![]() H2CO3+ OH-,其中由水电离出的c(OH-)等于溶液中氢氧根离子的浓度,即由水电离出的c(OH-)=10-3mol·L-1。
H2CO3+ OH-,其中由水电离出的c(OH-)等于溶液中氢氧根离子的浓度,即由水电离出的c(OH-)=10-3mol·L-1。
(3)根据图像可知,稀释相同倍数时,一元酸HX的pH变化量比HCl的小,这说明HX存在电离平衡,因此HX为弱酸。

练习册系列答案
相关题目