题目内容
【题目】已知苯可以进行如下转化,回答下列问题:
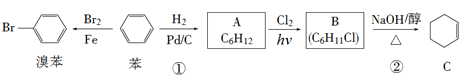
(1)反应①的反应类型为________,化合物A的化学名称为___________。
(2)化合物B的结构简式为_________,反应②的反应类型为__________。
(3)写出下列反应的化学方程式
A→B:_________________________。
B→C:_________________________。
【答案】加成反应 环己烷 ![]() 消去反应
消去反应 ![]()
![]()
【解析】
苯与液溴在Fe催化下发生取代反应产生溴苯![]() ,苯与H2在Pd/C催化下发生加成反应产生环己烷
,苯与H2在Pd/C催化下发生加成反应产生环己烷![]() ,环己烷与Cl2在光照条件下发生取代反应产生一氯环己烷
,环己烷与Cl2在光照条件下发生取代反应产生一氯环己烷![]() ,一氯环己烷与NaOH的乙醇溶液共热,发生消去反应产生环己烯
,一氯环己烷与NaOH的乙醇溶液共热,发生消去反应产生环己烯![]() 。
。
由上述分析可知A是![]() ,B是
,B是![]() 。
。
(1)反应①是![]() 与H2在Pd/C催化下发生加成反应产生环己烷
与H2在Pd/C催化下发生加成反应产生环己烷![]() ,反应类型为加成反应,化合物A是
,反应类型为加成反应,化合物A是![]() ,化学名称为环己烷。
,化学名称为环己烷。
(2)环己烷与Cl2在光照条件下发生取代反应产生化合物B是一氯环己烷,B的结构简式为![]() ,反应②是
,反应②是![]() 与NaOH的乙醇溶液共热,发生消去反应,产生
与NaOH的乙醇溶液共热,发生消去反应,产生![]() 、NaCl、H2O,该反应的反应类型为消去反应。
、NaCl、H2O,该反应的反应类型为消去反应。
(3)由(2)可知:A→B反应的化学方程式为:![]() 。B→C反应的化学方程式为:
。B→C反应的化学方程式为:![]() 。
。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】软锰矿的主要成分是MnO2,还含有少量金属铁、镁、铝、锌、铜的化合物等杂质。黄铁矿的主要成分是FeS2,还含有硅、铝的氧化物等杂质。工业上用软锰矿制备碳酸锰并回收硫酸铵,其主要流程如下:

已知金属离子从开始形成氢氧化物沉淀,到沉淀时溶液的pH如下表:
金属离子 | Fe2+ | Fe3+ | Al3+ | Cu2+ | Mn2+ |
开始沉淀pH | 7.5 | 2.7 | 4.1 | 5.9 | 8.8 |
完全沉淀pH | 9.5 | 3.7 | 5.4 | 6.9 | 10.8 |
(1)提高浸出率的可采取的措施有____。
a.适当升高温度 b.搅拌 c.加适量纯碱 d.加压
(2)浸取完成后,取浸取液少许,加入KSCN溶液无明显现象,则浸取时发生的主要反应的化学方程式是__________________________。
(3)调节pH为5.4~5.8的目的是______________。
(4)滤渣3的主要成分的化学式是_______。
(5)采用50℃碳化的原因是_________________________________。该过程发生反应的离子方程式是__________________。
(6)检验碳酸锰产品完全洗净的方法是_______________________________。
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是

选项 | ① | ② | ③ | 实验结论 |
A | 浓氨水 | NaOH | 酚酞试液 | 碱性:NaOH>NH3·H2O |
B | 浓硫酸 | 蔗糖 | 品红溶液 | 浓硫酸具有脱水性、氧化性 |
C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐反应均可生成白色沉淀 |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
A. A B. B C. C D. D