题目内容
某反应中反应物与生成物有:AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。(1)已知KBrO3在反应中得到电子,则该反应的还原剂是__________________。
(2)已知0.2 mol KBrO3在反应中得到1 mol电子生成X,则X的化学式为__________________。
(3)根据上述反应可推知__________________。
a.氧化性:KBrO3>H3AsO4
b.氧化性:H3AsO4>KBrO3
c.还原性:AsH3>X
d.还原性:X>AsH3
(4)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:
![]()
(1)AsH3 (2)Br2 (3)a c
(4) 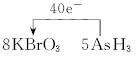
解析:(1)KBrO3在反应中得到电子,则另外一种化合价变化的元素在反应中失去电子被氧化,所给物质中AsH3中As元素失电子、化合价升高作为还原剂。
(2)0.2 mol KBrO3得到1 mol电子,说明Br元素在反应中降低了5价,所以X的化学式为Br2。
(4)利用氧化还原反应中电子得失相等的规律可配平该方程式为
 ====4K2SO4+4Br2+5H3AsO4+4H2O
====4K2SO4+4Br2+5H3AsO4+4H2O

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
某反应中反应物与生成物有: AsH3、H2SO4、KBrO3、K2SO4、H3AsO4、H2O和一种未知物质X。已知0.1mol KBrO3在反应中得到0.5mol电子生成X,则下列说法错误的是
| A.氧化产物与还原产物的计量系数之比为5:2 | B.氧化性:KBrO3>H3AsO4 |
| C.AsH3中As元素被氧化,发生氧化反应 | D.X的化学式为Br2 |
