题目内容
一容积恒定的密闭容器中盛有1mol PCl5,加热到200℃时发生反应:PCl5(g)![]() PCl3(g)+Cl2(g),反应达到平衡时,PCl5所占体积百分数为M%,若在同一温度下和同一容器中,最初投入的是2mol PCl5,反应达到平衡时,PCl5所占体积百分数为N%,则M和N的正确关系是( )
PCl3(g)+Cl2(g),反应达到平衡时,PCl5所占体积百分数为M%,若在同一温度下和同一容器中,最初投入的是2mol PCl5,反应达到平衡时,PCl5所占体积百分数为N%,则M和N的正确关系是( )
A. M>N B. M<N C. M=N D. 无法比较
B
解析:
两个容积相同的容器各装有1mol PCl5,建立完全相同的平衡状态,PCl5所占体积百分数为M%;以M%的两个状态(I)合并成过渡状态(Ⅱ),因外界条件不变,状态(Ⅱ)中PCl5的体积百分数仍为M%;恒温下加压,使状态(Ⅱ)体积缩小一半,则构成状态(Ⅲ),它相当于在原容器中加入2mol PCl5后达到的平衡状态。在状态(Ⅱ)→状态(Ⅲ)的过程中,因压强增加,状态(Ⅱ)中化学平衡向逆反应方向移动,PCl5的体积百分数增大,即N%>M%。其思路可用下图表示:


(14分)在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:
2SO2(g)+O2(g) 2SO3(g) △H=―190 kJ·mol—1
2SO3(g) △H=―190 kJ·mol—1
(1)该反应500℃时的平衡常数________450℃时的平衡常数(填“>”、“<”或“=”)。
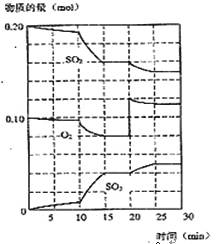
(2)450℃时,在一2L密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态的时间是 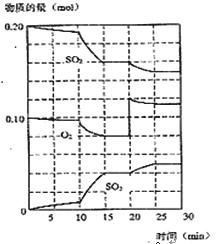
(3)据图判断,反应进行至20min时,曲线发生变化的原因是___________________(用文字表达),10min到15min的曲线变化的原因可能是 (填字母)。
| A.加了催化剂 | B.缩小容器体积 |
| C.降低温度 | D.增加SO3物质的量 |
(填字母)
a.向装置中再充入N2 b.向装置中再充入O2
c.改变反应的催化剂 d.升高温度
(5)利用图中数据计算450℃时反应进行至15min时,SO2的平衡转化率为: 。
(6)450℃时,另一2L容积不变的密闭容器中,测得某时刻各物质的量如下:
n(SO2)=0.4mol,n(O2)=0.2mol,n(SO3)=0.8mol,则此时该反应向 进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
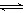 2SO3(g) △H=―190 kJ·mol—1
2SO3(g) △H=―190 kJ·mol—1 2SO3(g)
△H=―190 kJ·mol—1
2SO3(g)
△H=―190 kJ·mol—1