题目内容
已知:①向KMnO4晶体中滴加盐酸,产生黄绿色的气体;②向FeCl2溶液中通入少量的实验①产生的气体,溶液变黄色;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色。下列判断正确的是
A.上述实验证明氧化性:MnO4— > Cl2 > Fe3+ > I2
B.上述实验中发生的反应都是氧化—还原反应
C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝
D.实验②可以证明Fe2+既有氧化性又有还原性
AB
【解析】
试题分析:①向KMnO4晶体中滴加盐酸,产生黄绿色的气体,发生反应2KMnO4+16HCl(浓) = 2KCl+ 2MnCl2+5Cl2↑+8H2O,证明氧化性:MnO4— > Cl2;②向FeCl2溶液中通入少量的实验①产生的气体,溶液变黄色;发生反应:2Fe2++ Cl2=2 Fe3++2Cl-,说明氧化性:Cl2 > Fe3+;③取实验②生成的溶液滴在淀粉KI试纸上,试纸变蓝色,发生反应:2Fe3++2I-===2Fe2++I2. 说明氧化性:Fe3+ > I2,因此氧化性由强到弱的顺序是:MnO4— > Cl2 > Fe3+ > I2,故选项A正确;由于在上述反应中都有元素的化合价的变化,所以上述实验中发生的反应都是氧化—还原反应,选项B正确;氧化性强的可以把氧化性弱的氧化产生,因此实验①生成的气体Cl2能使湿润的淀粉KI试纸变蓝;选项C错误;D.在实验②Fe2+失去电子,表现诶还原性,因此不能证明Fe2+既有氧化性又有还原性,选项D错误。
考点:考查物质在氧化还原反应中的作用及氧化性强弱比较的知识。

(本题共10分)水煤气转化反应CO(g)+H2O(g)  CO2(g)+H2 (g)在一定温度下达到化学平衡。完成下列填空:
CO2(g)+H2 (g)在一定温度下达到化学平衡。完成下列填空:
29.写出该反应的平衡常数表达式K=________________。
30.一定温度下,在一个容积不变的密闭容器中发生上述反应,下列说法中能判断该反应达到化学平衡状态的是 (选填编号)。
A.容器中的压强不变
B.1 mol H―H键断裂的同时断裂2 molH―O键
C.v正(CO) = v逆(H2O)
D.c(CO) = c(H2)
31.将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中进行反应,得到如下实验1和实验2的数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | H2 | CO | |||
1 | 650 | 2 | 4 | 1.6 | 2.4 | 3 |
2 | 650 | 1 | 2 | 0.8 | 1.2 | 5 |
3 | 950 | 1 | 2 | — | — | — |
(1)由实验组1的数据可知,平衡时CO的转化率为 %。
(2)由实验组1和2的数据可分析,压强对该可逆反应的影响是 。
(3)有了实验组1和2的数据,再设计实验3,其目的是 。
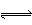 H+ + Cl– + HClO
H+ + Cl– + HClO
 O2(g) == H2O(1) △H= ―285.8kJ/mol
O2(g) == H2O(1) △H= ―285.8kJ/mol