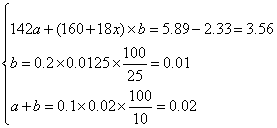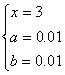题目内容
把Na2SO4、BaSO4和CuSO4•![]() H2O晶体组成的混合物5.89g,溶于水过滤,将所得沉淀洗净,烘干,冷却后称其质量为2.33g,所得滤液为100mL。取25mL用0.2mol•L-1的硫化钠溶液沉淀Cu2+,当Cu2+刚好完全沉淀时消耗硫化钠溶液体积为12.5mL;另取滤液10mL用0.1mol•L-1氯化钡溶液20mL刚好使溶液中的SO
H2O晶体组成的混合物5.89g,溶于水过滤,将所得沉淀洗净,烘干,冷却后称其质量为2.33g,所得滤液为100mL。取25mL用0.2mol•L-1的硫化钠溶液沉淀Cu2+,当Cu2+刚好完全沉淀时消耗硫化钠溶液体积为12.5mL;另取滤液10mL用0.1mol•L-1氯化钡溶液20mL刚好使溶液中的SO![]() 全部沉淀。
全部沉淀。
计算:(1)原混合物中Na2SO4的质量。 (2)CuSO4•![]() H2O中的
H2O中的![]() 值。
值。
答案:
解析:
解析:
沉淀为BaSO4 2.33g,反应方程式:CuSO4+Na2S== CuS↓+Na2SO4; SO 设 Na2SO4
解得 (1) m(Na2SO4)=142×0.01=1.42(g) (2)
(2)
|

练习册系列答案
相关题目
用一种试剂就可把Na2SO4、NH4NO3、KCl、(NH4)2SO4四种无色溶液加以鉴别(必要时可加热),此试剂是( )
| A、BaCl2溶液 | B、AgNO3溶液 | C、NaOH溶液 | D、Ba(OH)2溶液 |