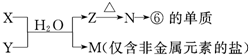
题目内容
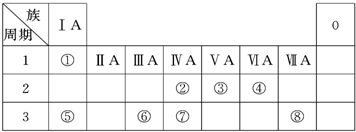
问题从周期表的第二、三周期的元素分析来看,位于同一周期元素的原子结构有什么相同之处?它们之间有没有递变规律?怎样递变?为什么有这种递变?
从周期表的第1、17列元素分析来看,同一列(族)元素的原子结构有什么相同之处?它们之间有没有递变规律?怎样递变?为什么有这种递变?
解析:
|
导思:要学会透过外在现象抓内在联系.关键要清楚讨论原子结构需要从哪几个角度来看,一般包含:核外电子排布(重点是电子层数、最外层电子数)、原子半径等内容. 关于原子半径的大小,则是要找到影响原子半径大小的因素,从以下几方面分析: 电子层数多少(层多径大)、核电荷数多少(核电荷数越多,半径越小)、电子数多少(核外电子数越多,半径越大),并要从中找出矛盾的主要方面,然后再来决定递变结果,即规律内容. 探究:从第二、三周期元素来看,同周期内元素的原子结构的相同点:电子层数相同,但有递变.递变规律:随着原子序数的递增,最外层电子数依次增加,从1增至8;原子半径依次减小,从第1列中的最大值递减到第17列的最小值,第18列例外.发生这个递变的原因是,同周期中,虽然电子数增多会使半径增大,但核电荷越多,核对外层电子的吸引力越大,使原子的内缩力增大,这个方面成为矛盾的主要方面,因此,原子半径越来越小. 而从第1、17列来看,同主族中,最外层电子数相等,但也有递变方面,即随着原子序数的递增,电子层数越来越多,原子半径越来越大.原因是:随着原子序数的递增,虽然核电荷数增大会使半径减小,但电子数的增多,特别是电子层数的增多使半径增大成了矛盾的主要方面. 电子层数相同.最外层电子数依次增加,从1增至8;原子半径依次减小.同主族中,最外层电子数相等,电子层数越来越多,原子半径越来越大. |

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案(13分)下表为元素周期表中前四周期的部分元素(从左到右按原子序数递增排列,部分涉及到的元素未给出元素符号),根据要求回答下列各小题:
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1)在以上表格中所有元素里基态原子的电子排布中4s轨道上只有1个电子的元素有 (填元素名称)。
(2)根据元素原子的外围电子排布的特征,可将元素周期表前四周期元素分成4个区域,分别为s区、p区、d区、ds区,,则属于s区的元素有 种,属于d区的元素有 种。第二周期元素中除Ne外电负性由高到低的三种元素依次是 ,电离能由高到低的三种元素依次是 。
(3)Mn、Fe均为第四周期过渡元素,两元素的部分电离能数据列于下表:
|
元素 |
Mn |
Fe |
|
|
电离能 ( kJ·mol-1) |
I1 |
717 |
759 |
|
I2 |
1509 |
1561 |
|
|
I3 |
3248 |
2957 |
回答下列问题:
Mn元素的电子排布式为____________________________________,
Fe2+的电子排布图为__________________________
比较两元素的I2、I3可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个 电子难。对此,你的解释是:_____________________________
【解析】(1)考查元素周期表的结构和原子核外电子的排布规律。根据构造原理可知4s轨道上只有1个电子的元素是K、Cr和 Cu。
(2)除ds区外,区的名称来自于构造原理最后填入电子的能级的符号,即s区包括第IA和ⅡA,共2列。p区包括第ⅢA到第 ⅦA以及0族,共6列。D区包括第3列到第10列,共8列。ds区包括第11和12列,共2列。非金属性越强,电负性越大,第一电离能也越大,非金属性是Cl>S>P,所以电负性是Cl>S>P。由于P原子的3p轨道属于半充满,属于第一电离能是Cl>P>S。
(3)根据构造原理可以写出锰元素的电子排布,即1s22s22p63s23p63d54s2,Fe2+的电子排布图为1s22s22p63s23p63d6。由于Mn2+的3d轨道属于半充满,比较稳定,所以再失去1个电子所需要的能量就高。而Fe2+的3d轨道上有6个电子,Fe3+的3d轨道上有5个电子,属于不充满比较稳定,因此3d能级由不稳定的3d6到稳定的3d5半充满状态,需要的能量相对要少。