题目内容
Cu、Mg合金15.2g全部溶解在一定量的浓NHO3中,生成标况下的NO2 6.72L和NO 2.24L求:①被还原的HNO3的物质的量;
②合金中铜、镁各多少克?
【答案】分析:从氧化还原反应得失电子守恒和质量守恒的角度计算相关物理量.
解答:解:设Cu,Mg分别为xmol和ymol
①
根据N守恒,被还原的HNO3为0.3mol+0.1mol=O.4mol,
答:被还原的HNO3的物质的量为0.4mol.
②
解得:x=0.2,y=0.1,m(Cu)=0.2mol×64g/mol=12.8g,m(Mg)=0.1mol×24g/mol=2.4g
答:合金中铜、镁的质量分别为12.8g、2.4g.
点评:本题考查混合物的计算,题目难度不大,注意从守恒的角度解答.
解答:解:设Cu,Mg分别为xmol和ymol
①

根据N守恒,被还原的HNO3为0.3mol+0.1mol=O.4mol,
答:被还原的HNO3的物质的量为0.4mol.
②

解得:x=0.2,y=0.1,m(Cu)=0.2mol×64g/mol=12.8g,m(Mg)=0.1mol×24g/mol=2.4g
答:合金中铜、镁的质量分别为12.8g、2.4g.
点评:本题考查混合物的计算,题目难度不大,注意从守恒的角度解答.

练习册系列答案
相关题目
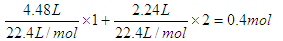 ,所以根据得失电子守恒可知,金属结合的氧原子是0.2mol,质量是0.2mol×16g/mol=3.2g,所以最终的固体质量是11.6g。即答案是B。
,所以根据得失电子守恒可知,金属结合的氧原子是0.2mol,质量是0.2mol×16g/mol=3.2g,所以最终的固体质量是11.6g。即答案是B。