题目内容
11.常温下,取铝热反应后所得固体(含有Al2O3、Fe、Fe2O3等物质)用过量稀硫酸浸出后的溶液,分别向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是( )| A. | 加入过量 NaOH 溶液:Na+、AlO2-、OH-、SO42- | |
| B. | 加入过量氨水:NH4+、Al3+、OH-、SO42- | |
| C. | 加入过量粉:Fe3+、H+、Al3+、SO42- | |
| D. | 加入过量 NaNO3 溶液:Fe2+、H+、NO3-、SO42- |
分析 加入过量硫酸溶解后过滤,滤液中含有的离子为:Fe2+、Al3+、SO42-、H+,若Fe不足,可能含有Fe3+,
A.加入过量氢氧化钠溶液,铁离子、亚铁离子生成沉淀,Al3+生成AlO2-;
B.加入过量粉,铁离子、氢离子与铁反应;
C.通入过量SO2,与铝离子不反应;
D.酸性条件下硝酸根离子能够氧化亚铁离子.
解答 解:加入过量硫酸溶解后过滤,滤液中含有的离子为:Fe2+、Al3+、SO42-、H+,若Fe不足,可能含有Fe3+,
A.加入过量NaOH溶液,Fe2+、Fe3+生成沉淀,Al3+生成AlO2-,溶液中含有离子为:Na+、AlO2-、OH-、SO42-,故A正确;
B.加入氨水,Al3+可生成氢氧化铝沉淀,且Al3+、OH-之间发生反应,不能共存,故B错误;
C.加入过量铁粉,Fe3+、H+与Fe反应,在溶液中不能大量存在,故C错误;
D.Fe2+、H+、NO3-之间发生氧化还原反应,在溶液中不能大量共存,故D错误.
故选A.
点评 本题考查离子共存,为高考的高频题,题目难度中等,明确滤液组成为解答关键,试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.

练习册系列答案
相关题目
2.现有下列试剂:(1)氯水 (2)Br2水 (3)碘水 (4)碘酒 溶液,其中能使淀粉碘化钾溶液变蓝的是( )
| A. | 除(3)外 | B. | 除(4)外 | C. | 除(2)外 | D. | 全部 |
19.有三种短周期的元素分别为X、Y和Z,已知X元素的原子价电子排布式为ns1,Y元素原子的K层电子是L层电子数的一半,Z元素原子K电子层上的电子数是L电子层上电子数的$\frac{1}{3}$,则这三种元素所组成的化合物的分子式不可能是( )
| A. | X2YZ | B. | X2YZ2 | C. | X2YZ3 | D. | X2YZ4 |
5.下列说法正确的是( )
| A. | 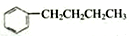 的与H2加成之后的产物中,其一氯代物有7种 的与H2加成之后的产物中,其一氯代物有7种 | |
| B. | CH3CH=CHCH3分子中的四个碳原子在同一直线上 | |
| C. | 按系统命名法,化合物 的名称是2,3,4-三甲基-2-乙基戊烷 的名称是2,3,4-三甲基-2-乙基戊烷 | |
| D. |  的一溴代物和 的一溴代物和  的一溴代物都有4种(不考虑立体异构) 的一溴代物都有4种(不考虑立体异构) |
2.关于下列各实验装置的叙述中,不正确的是( )


| A. | 图①可用于实验室制备少量Cl2或NH3 | |
| B. | 可用从a处加水的方法检验装置②的气密性 | |
| C. | 实验室也可以用装置③收集HCl气体 | |
| D. | 装置④可用于苯萃取碘水中碘的实验,并把碘的苯溶液从漏斗上口倒出 |
3.下列说法正确的是( )
| A. | 室温时,某溶液的 pH小于7,则该溶质一定是酸或强酸弱碱盐 | |
| B. | 室温时,0.1mol•L-1 一元酸 HA的电离平衡常数为1×10-7,则该酸电离度约为0.1% | |
| C. | 浓度均为 0.01mol•L-1 的 CH3COOH 溶液和 CH3COONa 溶液等体积混合,混合溶液中:(CH3COO- )+c(CH3COOH)=0.02 mol?L-1 | |
| D. | 在温度不变的情况下,向MgCO3饱和溶液中加入Na2CO3溶液,MgCO3 将会析出,但Ksp不变 |
 在水的电离平衡中,c(H+)和c(OH-)的关系如图所示:
在水的电离平衡中,c(H+)和c(OH-)的关系如图所示: