题目内容
(12分)Q、R、X、Y、Z五种元素的原子序数依次递增。已知:①Z的原子序数为29,其余的均为短周期主族元素;②Y原子价电子(外围电子)排布msnmpn ③R原子核外L层电子数为奇数;④Q、X原子p轨道的电子数分别为2和4。请回答下列问题:
(1)Z2+ 的核外电子排布式是
(2)Q与Y形成的最简单气态氢化物分别为甲、乙,下列判断正确的是 。
A.稳定性:甲>乙,沸点:甲>乙 B.稳定性:甲>乙,沸点:甲<乙
C.稳定性:甲<乙,沸点:甲<乙 D.稳定性:甲<乙,沸点:甲>乙
(3)Q、R、Y三种元素的第一电离能数值由小到大的顺序为 (用元素符号作答)。
(4)五种元素中,电负性最大与最小的两种非金属元素形成的化合物的化学式为 。
(5)Q的一种氢化物相对分子质量为28,其中分子中的σ键与π键的键数之比为 ,该氢化物与氧气形成的燃料电池在碱性电解质中负极反应为 。
(1)1s22s22p63s23p63d9 (2)B (3)Si<C<N (4)SiO2
(5)5:1;C2H4-12e-+16OH-=2CO32020+10H2O
【解析】
试题分析:Z的原子序数为29,则Z为Cu元素;Q、R、X、Y均为短周期主族元素,Q、R、X、Y、Z五种元素的原子序数依次递增。Q、X的p轨道为2和4,则为Q为C元素和X为O元素;Y原子价电子(外围电子)排布msnmpn,s能级容纳电子数为2,则Y可能为C或Si,由于Q为C元素,所以Y为Si元素;R的核外L层为奇数,所以R有2个电子层,则可能为Li、B、N或F,R的原子序数介于Q与X之间,Q为C元素,X为O元素,则R为N元素,所以可推出:Q为C,R为N,X为O,Y为Si,Z为Cu,则
(1)Z为Cu元素,Z2+为Cu2+,Cu的价电子排布为3d104s1,失去两个电子,则为3d9,Cu2+的核外电子排布式是1s22s22p63s23p63d9;
(2)Q、Y的氢化物分别为CH4和SiH4,由于C的非金属性强于Si,则稳定性CH4>SiH4.因为SiH4 的相对分子质量比CH4大,故分子间作用力大,沸点高,故选:B;
(3)C、N和Si中,C、Si位于同一主族,则上面的非金属性强,故第一电离能大,即Si<C,而N由于具有半充满状态,故第一电离能比相邻元素大,C<N,所以第一电离能Si<C<N。
(4)电负性最大的非金属元素是O,最小的非金属元素是Si,两者构成SiO2;
(5)Q为C元素,C、H形成的相对分子质量为28的物质为C2H4,结构式为 ,单键是σ键,双键中有一个是σ键一个π键,所以σ键与π键数之比为5:1。在乙烯与氧气形成的碱性燃料电池中乙烯在负极通入,失去电子,电极反应式为C2H4-12e-+16OH-=2CO32020+10H2O。
,单键是σ键,双键中有一个是σ键一个π键,所以σ键与π键数之比为5:1。在乙烯与氧气形成的碱性燃料电池中乙烯在负极通入,失去电子,电极反应式为C2H4-12e-+16OH-=2CO32020+10H2O。
考点:考查物质结构与性质、核外电子排布、电离能、化学键、燃料电池等

 字词句段篇系列答案
字词句段篇系列答案(10分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
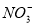 +4H++3e-=NO+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
+4H++3e-=NO+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:______________。
(2)反应中硝酸体现了________、_________的性质。
(3)反应中若产生0.2 mol气体,则转移电子的物质的量是___________mol。
(4)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是___________。
下列有关微粒之间关系和特征描述正确的是( )。
选项 | 微粒 | 相互关系 | 特征描述 |
A | C60、C70、C540 | 同位素 | 微粒中只含非极性共价键 |
B | 新戊烷、2,2-二甲基丙烷 | 同分异构体 | 常温常压下呈气态 |
C | 同素异形体 | 铂作氨催化氧化时的催化剂 | |
D | 甲酸、硬脂酸 | 同系物 | 能发生酯化反应 |
为探究NaHCO3、Na2CO3与1mol·L-1盐酸反应(设两反应分别是反应Ⅰ、反应Ⅱ)过程中的热效应,进行实验并测得如下数据:
序号 | 液体 | 固体 | 混合前温度 | 混合后最高温度 |
① | 35 mL水 | 2.5g NaHCO3 | 20℃ | 18.5℃ |
② | 35 mL水 | 3.2g Na2CO3 | 20℃ | 24.3℃ |
③ | 35 mL盐酸 | 2.5g NaHCO3 | 20℃ | 16.2℃ |
④ | 35 mL盐酸 | 3.2g Na2CO3 | 20℃ | 25.1℃ |
下列有关说法正确的是
A.仅通过实验③即可判断反应Ⅰ是吸热反应
B.仅通过实验④即可判断反应Ⅱ是放热反应
C.通过实验可判断出反应Ⅰ、Ⅱ分别是吸热反应、放热反应
D.通过实验可判断出反应Ⅰ、Ⅱ分别是放热反应、吸热反应


 ===BaCO3↓+CO
===BaCO3↓+CO +2H2O
+2H2O