题目内容
下列四种溶质溶于水后,所得溶液中,没有溶质分子的是( )
| A、NaOH |
| B、NH4OH |
| C、CH3COOH |
| D、SO2 |
考点:电解质在水溶液中的电离
专题:
分析:根据强电解质全部电离,弱电解质部分电离来分析;
解答:
解:A、NaOH属于强碱强电解质,在水溶液中全部电离,所以不存在溶质分子,故A正确;
B、NH4OH属于弱碱弱电解质,在水溶液中部分电离,所以存在溶质分子,故B错误;
C、醋酸属于弱电解质,在水溶液中部分电离,所以存在溶质分子,故C错误;
D、二氧化硫溶于水,与水反应生成亚硫酸,属于弱酸,在水溶液中部分电离,所以存在溶质分子,故D错误;
故选:A.
B、NH4OH属于弱碱弱电解质,在水溶液中部分电离,所以存在溶质分子,故B错误;
C、醋酸属于弱电解质,在水溶液中部分电离,所以存在溶质分子,故C错误;
D、二氧化硫溶于水,与水反应生成亚硫酸,属于弱酸,在水溶液中部分电离,所以存在溶质分子,故D错误;
故选:A.
点评:主要考查了强电解质全部电离,弱电解质部分电离,比较基础,记住常见的强弱电解质即可.

练习册系列答案
相关题目
铜锌原电池(如图)工作时,下列叙述不正确的是( )
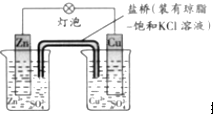

| A、撤掉盐桥不能形成闭合回路,所以不能形成原电池 |
| B、电池反应为Zn+Cu2+═Zn2++Cu |
| C、在外电路中,电子从负极流向正极 |
| D、每生成1molCu,通过盐桥的电子为2mol |
现有甲、乙、丙、丁和Fe(OH)3等五种胶体,按甲和丙、乙和丁、丙和丁、乙和胶体Fe(OH)3两两混合,均出现胶体聚沉现象.则粒子带负电荷的胶体是( )
| A、甲和乙 |
| B、丙和乙 |
| C、甲和丁 |
| D、丙和Fe(OH)3胶体 |
下列物质都能导电,其中属于电解质的是( )
| A、熔融的NaOH | B、铁丝 |
| C、稀硫酸 | D、NaCl溶液 |
有机物A可氧化为B(分子式为C2H3O2Br),而A水解得到C,1molC和2molB反应可得到含Br的酯D(分子式为C6H8O4Br2),由此推断A的结构简式为( )
| A、BrCH2CH2OH |
| B、BrCH2CHO |
| C、HOCH2CH2OH |
| D、BrCH2COOH |
 在一定条件下可实现如图所示物质之间的变化:
在一定条件下可实现如图所示物质之间的变化: