题目内容
已知下列热化学方程式:
①H2(g)+![]() O2(g)
O2(g)![]() H2O(l)ΔH=-285.8 kJ·mol-1
H2O(l)ΔH=-285.8 kJ·mol-1
②H2(g)+![]() O2(g)
O2(g)![]() H2O(g)ΔH=-241.8 kJ·mol-1
H2O(g)ΔH=-241.8 kJ·mol-1
③C(s)+![]() O2(g)
O2(g)![]() CO(g)ΔH=-110.5 kJ·mol-1
CO(g)ΔH=-110.5 kJ·mol-1
④C(s)+O2(g)![]() CO2(g)ΔH=-393.5 kJ·mol-1
CO2(g)ΔH=-393.5 kJ·mol-1
回答下列各问题:
(1)上述反应中属于放热反应的是_________.
(2)H2的燃烧热为_________;C的燃烧热为_________.
(3)燃烧10 g H2生成液态水,放出的热量为_________.
(4)CO的燃烧热为_________;其热化学方程式为_________.
答案:
解析:
解析:
(1)①②③④
(2)285.8 kJ·mol-1 393.5 kJ·mol-1
(3)1 429 kJ
(4)283 kJ·mol-1 CO(g)+12O2(g)![]() CO2(g) ΔH=-283 kJ·mol-1
CO2(g) ΔH=-283 kJ·mol-1

练习册系列答案
 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
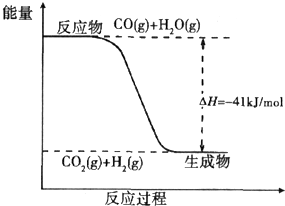 煤炭可以转化为清洁能源和化工原料.
煤炭可以转化为清洁能源和化工原料.