��Ŀ����
��1����֪���淴Ӧ��M(g)��N(g)![]() P(g)��Q(g) ��H��0��
P(g)��Q(g) ��H��0��
��Ҫ����Q��Ũ�ȣ��������������������¿��Բ�ȡ�Ĵ�ʩΪ ������ţ���
A������һ����M B�����ͷ�Ӧ�¶� C�����߷�Ӧ�¶�
D����С������� E��������� F�������һ����P
��2����˹�����������Ϳ�ѧ�о����к���Ҫ�����塣��Щ��Ӧ�ķ�Ӧ����Ȼ��ֱ�Ӳ�ã�����ͨ����ӵķ����ⶨ���ָ�������3���Ȼ�ѧ��Ӧ����ʽ��
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ��H����24.8 kJ��mol��1
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) ��H����47.2 kJ��mol��1
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) ��H����640.5 kJ��mol��1
д��CO���廹ԭFeO����õ�Fe �����CO2������Ȼ�ѧ��Ӧ����ʽ��
_________________ ��
��3�������Ϊ1 L���ܱ������У�����1 mol CO2��3 mol H2��һ�������·�����Ӧ�� CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) ��H=��49.0 kJ/mol�� ��
CH3OH(g)+H2O(g) ��H=��49.0 kJ/mol�� ��
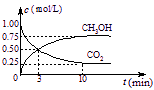 ��CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ��
��CO2��CH3OH(g)��Ũ����ʱ��仯����ͼ��ʾ��
�ٴ�3 min��10 min��v(H2)= mol/(L��min)��
����˵��������Ӧ�ﵽƽ��״̬���� ��ѡ���ţ���
A����Ӧ��CO2��CH3OH�����ʵ���Ũ��֮��Ϊ1�U1����ͼ�н���㣩
B�����������ܶȲ���ʱ��ı仯���仯
C����λʱ����ÿ����3 mol H2��ͬʱ����1 mol H2O
D��CO2����������ڻ�������б��ֲ���
�����д�ʩ����ʹn (CH3OH)/n (CO2)������� ��ѡ���ţ���
A�������¶� B�����º��ݳ���He(g)
C����H2O(g)����ϵ�з��� D�����º����ٳ���1 mol CO2��3 mol H2
��1��A C D F��2�֣�
��2��CO(g)+FeO(s)= Fe(s) + CO2(g) ��H=??��218.00 kJ��mol��1��2�֣�
��3�� ��0.11��![]() ����D ��CD ��ÿ��2�֣�
����D ��CD ��ÿ��2�֣�

 ��2011?���϶�ģ����1����֪���淴Ӧ��M��g��+N��g��
��2011?���϶�ģ����1����֪���淴Ӧ��M��g��+N��g�� P��g��+Q��g������H��0����ش��������⣺
P��g��+Q��g������H��0����ش��������⣺
 HCl+HClO������ˮ�м���NaHCO3�������Һ��HClO��Ũ�� ��������С�����䣩��ԭ���ǣ� ��
HCl+HClO������ˮ�м���NaHCO3�������Һ��HClO��Ũ�� ��������С�����䣩��ԭ���ǣ� �� 2���ĺ���Ӧ������0.2mg��L��1����pH��2.0ʱ�� ClO2���ܱ�I����ԭ��Cl������д����Ӧ�����ӷ���ʽ ��
2���ĺ���Ӧ������0.2mg��L��1����pH��2.0ʱ�� ClO2���ܱ�I����ԭ��Cl������д����Ӧ�����ӷ���ʽ �� P(g)��Q(g)����H��0����ش��������⣺
P(g)��Q(g)����H��0����ش��������⣺