题目内容
(1)路布兰法是以食盐、石灰石、浓硫酸、焦炭为原料,在高温下进行煅烧,再浸取、结晶而制得纯碱。
①食盐和浓硫酸反应的化学方程式为____________________;
②硫酸钠和焦炭、石灰石反应的化学方程式为_______________ (已知产物之一为CaS);
(2)氨碱法的工艺如下图所示,得到的碳酸氢钠经煅烧生成纯碱。
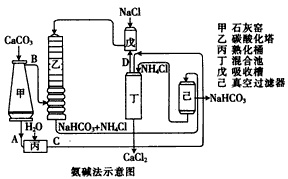
②装置乙中发生反应的化学方程式为_____________________;
(3)联合制碱法是对氨碱法的改进,其优点是___________________;
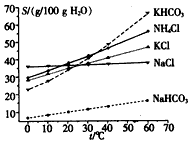
(4)有人认为碳酸氢钾与碳酸氢钠的化学性质相似,故也可用氨碱法以氯化钾和石灰石等为原料制碳酸钾。请结合下图的溶解度(S)随温度变化曲线,分析说明是否可行?________________________
(1)①2NaCl+H2SO4(浓) Na2SO4+2HCl;②Na2SO4+4C+CaCO3
Na2SO4+2HCl;②Na2SO4+4C+CaCO3 CaS+Na2CO3+4CO
CaS+Na2CO3+4CO
(2)①Ca(OH)2;NH3;②NH3+CO2+NaCl+H2O=NaHCO3+NH4Cl
(3)保留了氨碱法的优点,使食盐的利用率提高到96%,NH4Cl可做氮肥,可与合成氨厂联合,原料气氨气和一氧化碳都由氨厂提供,减少CaCO3制CO2这一工序,降低了能耗与污染。
(4)不可行,因为在纯碱的生产中,生成的碳酸氢钠溶解度小于氯化钠,故生产中能以晶体析出而分离。但若用于碳酸钾的生产,将会生成碳酸氢钾,其溶解度要远小于氯化钠,必须在温度接近0℃时才能结晶,能耗过大,工业上不可行。

氯碱工业中,通过电解饱和食盐水获得重要的化工原料:氯气、氢气和氢氧化钠。其中氯气用途十分广泛,除用于净水、环境消毒外,还用于生产盐酸、硅、聚氯乙烯、氯苯等。
(1)写出工业上制取盐酸的化学反应方程式:
(2)工业上可用氯气和石灰乳为原料制造漂白粉,写出漂白粉在空气中的漂白原理(用化学方程式表示) 。
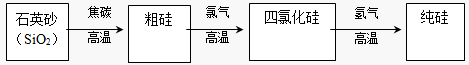
(3)工业上生产半导体材料硅的流程如下: 
①写出在制备粗硅时反应的化学方程式_____________________________,此反应中焦炭的作用是____________(填“氧化剂”或“还原剂”),若有 0.6mol硅生成,反应中转移电子的物质的量是 mol。
②粗硅与氯气反应后得到沸点较低的液态四氯化硅中常混有一些高沸点,难挥发性杂质,必须进行分离提纯。其提纯方法为____________。(填序号)
| A.蒸馏 | B.过滤 | C.萃取 | D.结晶 |
________________________________________________________________________。