��Ŀ����
(16��) ��ѭ���ֽ�ˮ������Ҫ�漰���з�Ӧ��
I SO2+2H2O+I2==H2SO4+2HI
II 2HI  H2+I2
H2+I2
III 2H2SO4==2SO2+O2+2H2O
��1������������Ӧ�������ж���ȷ���� ��
a����ӦIII���ڳ����½���
b����ӦI��SO2�����Ա�HIǿ
c��ѭ���������貹��H2O
d��ѭ�������в���1molO2��ͬʱ����1 molH2
��2��һ���¶��£���1L�ܱ������м���1molHI��g����������ӦII��H2���ʵ�����ʱ��ı仯��ͼ��ʾ��0~2min�ڵ�ƽ����Ӧ����v��HI��= �����¶��£�H2��g��+I2��g�� 2HI��g����ƽ�ⳣ��K= ����ͬ�¶��£�����ʼ����HI��g�������ʵ�����ԭ����2������ ��ԭ����2����
2HI��g����ƽ�ⳣ��K= ����ͬ�¶��£�����ʼ����HI��g�������ʵ�����ԭ����2������ ��ԭ����2����
a��ƽ�ⳣ�� b��HI��ƽ��Ũ��
c���ﵽƽ���ʱ�� d��ƽ��ʱH2���������
��3��ʵ������Zn��ϡ������ȡH2����Ӧʱ��Һ��ˮ�ĵ���ƽ�� �ƶ�����������ҡ������������������������Լ��е� ������H2�����ʽ�����
a��NaNO3 b��CuSO4 c��Na2SO4 d��NaHSO3
��4����H2Ϊȼ�Ͽ���������ȼ�ϵ�ء�
��֪ 2H2��g��+O2��g��====2H2O��l�� ��H=-572kJ��mol-1
ij����ȼ�ϵ���ͷ�22.8kJ����ʱ������1molҺ̬ˮ���õ�ص�����ת����Ϊ ��
(16��)��1��c��2�֣�
��2��0.1mol��L��1��min��1��2�֣���64��3�֣���b��2�֣�
��3�����ң�2�֣���b��2�֣� ��4��80%��3�֣�
����

 ÿ��10���ӿ�����������������ϵ�д�
ÿ��10���ӿ�����������������ϵ�д�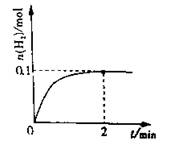
 H2+I2 ��.2H2SO4===2SO2+O2+2H2O
H2+I2 ��.2H2SO4===2SO2+O2+2H2O
 H2+I2 ��.2H2SO4===2SO2+O2+2H2O
H2+I2 ��.2H2SO4===2SO2+O2+2H2O
 H2+I2
H2+I2