题目内容
9.A、B、C、D、E为五种气态烃,其中A、B、C都能使酸性KMnO4褪色,1molC与2molBr2完全加成,生成物分子中每个碳原子都有一个溴原子,A与C通式相同,A与H2加成可得到B,B与N2密度相同,D是最简单的有机物,E为D的同系物,完全燃烧等摩尔B、E,生成CO2相同,试确定A、B、C、D、E的结构简式并作出简要说明.分析 A、B、C、D、E为五种气态烃,D是最简单的有机物,则D为甲烷;1molC与2molBr2完全加成,生成物分子中每个碳原子都有一个溴原子,则C含有4个C原子,为1,3-丁二烯与溴发生加成反应;A与C通式相同,A与H2加成可得到B,B与N2密度相同,则B的相对分子质量为28,故B为乙烯、A为乙炔;E为D的同系物,属于烷烃,完全燃烧等摩尔B、E,生成CO2相同,则E分子中含有2个C原子,故E为乙烷,以此解答该题.
解答 解:A、B、C、D、E为五种气态烃,D是最简单的有机物,则D为甲烷,结构简式为CH4;
1molC与2molBr2完全加成,生成物分子中每个碳原子都有一个溴原子,则C含有4个C原子,为1,3-丁二烯与溴发生加成反应,C为CH2=CH-CH=CH2;
A与C通式相同,A与H2加成可得到B,B与N2密度相同,则B的相对分子质量为28,故B为乙烯、A为乙炔,A的结构简式为CH≡CH、B的结构简式为CH2=CH2;
E为D的同系物,属于烷烃,完全燃烧等摩尔B、E,生成CO2相同,则E分子中含有2个C原子,故E为乙烷,结构简式为CH3CH3,
答:A、B、C、D、E的结构简式分别为CH≡CH、CH2=CH2、CH2=CH-CH=CH2、CH4、CH3CH3.
点评 本题考查有机物的推断,为高频考点,涉及烃的性质与组成、同系物、烃燃烧问题,难度不大,侧重对基础知识的巩固.

练习册系列答案
相关题目
19.下列排列顺序不正确的是( )
| A. | 原子半径:Na>S>O | B. | 酸性:H3PO4>H2SO4>HClO4 | ||
| C. | 热稳定性:HF>HCl>HBr | D. | 元素金属性:Na>Mg>Al |
17.下列说法正确的是( )
| A. | F是最活泼非金属,Li是最活泼金属 | |
| B. | X2+的核外电子数目为18,则X在第四周期第ⅡA族 | |
| C. | 元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16个纵行 | |
| D. | NaOH易溶于水,Ca(OH)2微溶,所以NaOH碱性比Ca(OH)2强 |
14.电解质溶液有许多奇妙之处,你只有深入思考,才能体会到它的乐趣.下列关于电解质溶液的叙述中正确的是( )
| A. | 常温下,某溶液中由水电离出的c(H+)=10-5 mol•L-1,则此溶液可能是盐酸 | |
| B. | pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液,NH4+大小顺序为:①>②>③ | |
| C. | 0.2 mol•L-1 CH3COOH溶液与0.1 mol•L-1 NaOH溶液等体积混合: c(H+)-c(OH-)=c(CH3COO-)-c(CH3COOH) | |
| D. | 0.1 mol•L-1 NaHCO3溶液中:c(Na+)+c(H+)+c(H2CO3)>c(HCO3-)+c(CO32-)+c(OH-) |

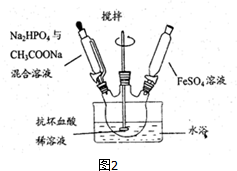
 ;
;
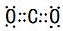 .
.