题目内容
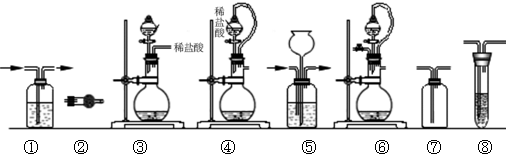
实验室常用强氧化剂(如KMnO4、KClO3、MnO2等)氧化浓盐酸的方法来制备氯气.某研究性学习小组欲探究用Na2O2与浓盐酸制备并检验氯气.供选用的实验试剂及装置如下(部分导管、蒸馏水略):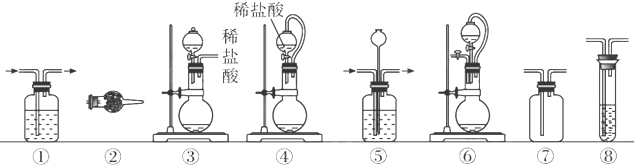
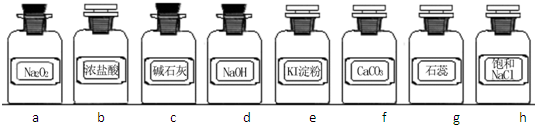
a、Na2O2 b、浓盐酸 c、碱石灰 d、NaOH溶液 e、淀粉-KI溶液 f、CaCO3
g、石蕊试液 h、饱和NaCl溶液
(1)写出用Na2O2与浓盐酸制备氯气的化学方程式
(2)下列装置组合最合理的是
(3)尾气经处理后仍有较多气体排出,其主要原因可用化学方程式表示为:
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
①
②

a、Na2O2 b、浓盐酸 c、碱石灰 d、NaOH溶液 e、淀粉-KI溶液 f、CaCO3
g、石蕊试液 h、饱和NaCl溶液
(1)写出用Na2O2与浓盐酸制备氯气的化学方程式
Na2O2+4HCl═2NaCl+Cl2↑+2H2O
Na2O2+4HCl═2NaCl+Cl2↑+2H2O
.(2)下列装置组合最合理的是
D
D
(填序号,需考虑实验结束撤除装置时残留有害气体的处理).| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③⑥ | ① | ⑧/g | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ⑥ | ⑤ | ⑧/g | ① |
2Na2O2+2H2O═4NaOH+O2↑
2Na2O2+2H2O═4NaOH+O2↑
.(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
①
Na2O2能与水反应,会使原料的利用率降低
Na2O2能与水反应,会使原料的利用率降低
,②
双氧水比Na2O2更经济
双氧水比Na2O2更经济
.分析:(1)过氧化钠具有强氧化性,能把浓盐酸氧化为氯气,同时自身被还原成水,再结合原子守恒写出反应方程式;
(2)根据反应物的性质选取反应装置,根据气体的成分及性质选取洗气装置,根据实验目的选取检验装置,根据氯气的性质选取尾气处理装置;
(3)根据过氧化钠的性质分析;
(4)从原料的利用率、成本、过氧化钠的性质及生成气体的性质来分析.
(2)根据反应物的性质选取反应装置,根据气体的成分及性质选取洗气装置,根据实验目的选取检验装置,根据氯气的性质选取尾气处理装置;
(3)根据过氧化钠的性质分析;
(4)从原料的利用率、成本、过氧化钠的性质及生成气体的性质来分析.
解答:解:(1)过氧化钠有强氧化性能把浓盐酸氧化生成氯气,同时自身被还原生成水,结合原子守恒写出其反应方程式为:Na2O2+4HCl=2NaCl+Cl2↑+2H2O,
故答案为:Na2O2+4HCl=2NaCl+Cl2↑+2H2O;
(2)用过氧化钠和浓盐酸制取氯气,反应物状态是固液混合,所以盛放液体用分液漏斗,易控制流量,浓盐酸挥发性较强,所以要采用密封装置,防止其挥发,利用产生气体的压强时盐酸流下,所以反应装置选④⑥;
浓盐酸具有挥发性,所以产生的气体中含有氯化氢,用饱和食盐水洗气,为防止洗气瓶内压强过大,应有一个缓冲装置,故选⑤;
用淀粉碘化钾溶液检验氯气,故选⑧;
氯气有毒不能直接排空,应该用氢氧化钠溶液吸收尾气,且尾气量较少,不需要缓冲装置即可,故选①,
故答案为:D;
(3)过氧化钠极易和水反应生成氧气,过氧化钠也能把浓盐酸氧化生成氯气,自身被还原为氧气,所以制取的气体中可能含有氧气,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑(或4Na2O2+4HCl=4NaCl+2H2O+O2↑),
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(4)从原料的利用率、成本、过氧化钠的性质及生成气体的性质来来考虑,所以其理由是:①Na2O2能与水反应,会使原料的利用率降低;②双氧水比Na2O2更经济,
故答案为:Na2O2能与水反应,会使原料的利用率降低;双氧水比Na2O2更经济.
故答案为:Na2O2+4HCl=2NaCl+Cl2↑+2H2O;
(2)用过氧化钠和浓盐酸制取氯气,反应物状态是固液混合,所以盛放液体用分液漏斗,易控制流量,浓盐酸挥发性较强,所以要采用密封装置,防止其挥发,利用产生气体的压强时盐酸流下,所以反应装置选④⑥;
浓盐酸具有挥发性,所以产生的气体中含有氯化氢,用饱和食盐水洗气,为防止洗气瓶内压强过大,应有一个缓冲装置,故选⑤;
用淀粉碘化钾溶液检验氯气,故选⑧;
氯气有毒不能直接排空,应该用氢氧化钠溶液吸收尾气,且尾气量较少,不需要缓冲装置即可,故选①,
故答案为:D;
(3)过氧化钠极易和水反应生成氧气,过氧化钠也能把浓盐酸氧化生成氯气,自身被还原为氧气,所以制取的气体中可能含有氧气,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑(或4Na2O2+4HCl=4NaCl+2H2O+O2↑),
故答案为:2Na2O2+2H2O=4NaOH+O2↑;
(4)从原料的利用率、成本、过氧化钠的性质及生成气体的性质来来考虑,所以其理由是:①Na2O2能与水反应,会使原料的利用率降低;②双氧水比Na2O2更经济,
故答案为:Na2O2能与水反应,会使原料的利用率降低;双氧水比Na2O2更经济.
点评:本题考查性质实验方案设计,要根据物质的性质来设计实验,要遵循“可行性、科学性、经济性、环保性”规律,难度较大.

练习册系列答案
 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案
相关题目
实验室常用强氧化剂(如KMnO4、KClO3和MnO2等)氧化浓盐酸的方法来制备氯气.某研究性学习小组欲探究用Na2O2与浓盐酸反应制备并检验氯气.供选用的实验试剂:a.Na2O2、b.浓盐酸、c.碱石灰、d.NaOH溶液、e.淀粉-KI溶液、f.CaCO3、g.石蕊试液、h.饱和NaCl溶液,装置如图所示(部分导管、蒸馏水略):
(1)写出用Na2O2与浓盐酸反应制备氯气的化学方程式: .
(2)下列装置组合最合理的是 (填序号,需考虑实验结束后拆卸装置时残留有害气体的处理).
(3)尾气经处理后仍有较多气体排出,其主要原因可用化学方程式表示为 .
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:① ,② .
(5)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一? (填“是”、“否”),理由是 .

(1)写出用Na2O2与浓盐酸反应制备氯气的化学方程式:
(2)下列装置组合最合理的是
| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③ | ① | ⑧/e | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ⑥ | ⑤ | ⑧/e | ① |
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:①
(5)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一?
实验室常用强氧化剂(如KMnO4、KClO3、MnO2等)氧化浓盐酸的方法来制备氯气.某研究性学习小组欲探究用Na2O2与浓盐酸制备并检验氯气.供选用的实验试剂及装置如下(部分导管、蒸馏水略):
a、Na2O2 b、浓盐酸 c、碱石灰 d、NaOH溶液 e、淀粉-KI溶液
f、CaCO3g、石蕊试液 h、饱和NaCl溶液

(1)写出实验室用二氧化锰和浓盐酸反应制备氯气的离子方程式
(2)写出用Na2O2与浓盐酸制备氯气的化学方程式 .该反应中盐酸的作用是
(3)下列装置组合最合理的是 (填序号,需考虑实验结束撤除装置时残留有害气体的处理).
(4)尾气经处理后仍有较多气体排出,其主要原因可用化学方程式表示为: .
(5)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
① ,
② .
a、Na2O2 b、浓盐酸 c、碱石灰 d、NaOH溶液 e、淀粉-KI溶液
f、CaCO3g、石蕊试液 h、饱和NaCl溶液

(1)写出实验室用二氧化锰和浓盐酸反应制备氯气的离子方程式
(2)写出用Na2O2与浓盐酸制备氯气的化学方程式
(3)下列装置组合最合理的是
| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③⑥ | ① | ⑧/g | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ⑥ | ⑤ | ⑧/g | ① |
(5)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
①
②
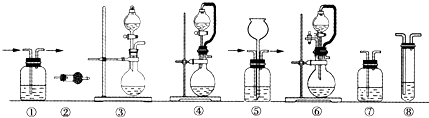
(12分)实验室常用强氧化剂(如KMnO4、KClO3、MnO2等)氧化浓盐酸的方法来制备氯气。某研究性学习小组欲探究用Na2O2与浓盐酸制备并检验氯气。供选用的实验试剂及装置如下(部分导管、蒸馏水略):
(1)写出用Na2O2与浓盐酸制备氯气的化学方程式_________________________。
(2)下列装置组合最合理的是__________ (填序号,需考虑实验结束撤除装置时残留有害气体的处理)。
| 组合 | 制备装置 | 净化装置 | 检验装置/试剂 | 尾气处理装置 |
| A | ③ | ② | ⑦/e | ⑤ |
| B | ③、⑥ | ① | ⑧/g | ① |
| C | ④ | ① | ⑤/e | ② |
| D | ④、⑥ | ⑤ | ⑧/g | ① |
(3)尾气经处理后仍有较多气体排出,其主要原因可用化学方程式表示为:____________ 。
(4)某小组成员建议用双氧水代替过氧化钠进行实验更好,请你给出两条合适的理由:
① ___________________________________,② ___________________________________。
(5)你是否同意将Na2O2与浓盐酸的反应作为实验室制备氯气的方法之一?___________(填“是”或“否”);理由是__________________________________________ 。