题目内容
L、M、N是原子序数小于20的元素,其原子序数依次增大,其中L、N能形成自然界中含量最多、存在最广泛的共价化合物L2N,L、M也能结合ML4型共价化合物.试回答:(1)M、N形成的常见化合物是______、______(写化学式)
(2)下列物质中,L、M、N三种元素能结合而成的是______(填选项编号)
a.L3MN4 b.L2MO3
c.M2L6N d.M2L4O2
解析:
| 答案:(1)CO CO2 (2)bcd
|
提示:
| 提示:自然界中存在最广泛含量最多的物质是H2O,则L为H元素,N为O元素.由化合物ML4,可知M为C元素.
乙醇和乙酸都是初中学过的内容,其化学式分别为C2H6O和C2H4O2.
|

 阅读快车系列答案
阅读快车系列答案
| |||||||||||||||
(18分)X、Y、Z、L、M、N六种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。回答下列问题:
(1)L的原子结构示意图为 ;M在元素周期表中的位置为 ;前五种元素的原子半径从大到小的顺序是 (用元素符号表示)。Z、L两元素的第一电离能大小关系为: > (填写元素符号),原因 。
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的分子构型为 ,B的结构式为 。
(3)N是人体必需的微量元素,与L同一主族,N原子比L原子多两个电子层,则N的电子排布式为 ,其最高价氧化物对应的水化物化学式为 。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下,表示生成1mol H2N反应热的是__________(填字母代号)。
| A.+99.7 mol·L-1 | B.+29.7 mol·L-1 |
| C.-20.6 mol·L-1 | D.-241.8 kJ·mol-1 |
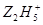 将Fe3+还原为Fe2+,
将Fe3+还原为Fe2+,