题目内容
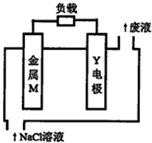 锌、铁、镁、铝、锂等金属都可以用在金属燃料电池中,电池的基本结构如图所示.下列说法正确的是( )
锌、铁、镁、铝、锂等金属都可以用在金属燃料电池中,电池的基本结构如图所示.下列说法正确的是( )分析:A、电子不能在电解液中移动;
B.若M为铝,电池总的化学方程式为4Al+302+3H2O=4Al(OH)3,依此分析溶液的PH变化;
C.若M为镁,电池总的化学方程式为2Mg+02+2H2O=2Mg(OH)2;
D.若M为铁,则负极Fe失去电子生成二价铁离子.
B.若M为铝,电池总的化学方程式为4Al+302+3H2O=4Al(OH)3,依此分析溶液的PH变化;
C.若M为镁,电池总的化学方程式为2Mg+02+2H2O=2Mg(OH)2;
D.若M为铁,则负极Fe失去电子生成二价铁离子.
解答:解:A、电子只在金属导线中移动,不能在电解液中移动,故A错误;
B.电解质溶液为NaCl溶液,呈中性,若M为铝,电池总的化学方程式为4Al+302+3H2O=4Al(OH)3,溶液的PH基本不变,故B错误;
C.电解质溶液为NaCl溶液,呈中性,若M为镁,电池总的化学方程式为2Mg+02+2H2O=2Mg(OH)2;故C错误;
D.若M为铁,则负极Fe失去电子生成二价铁离子,则负极的电极反应式为Fe-2e-=Fe2+,故D正确;
故选D.
B.电解质溶液为NaCl溶液,呈中性,若M为铝,电池总的化学方程式为4Al+302+3H2O=4Al(OH)3,溶液的PH基本不变,故B错误;
C.电解质溶液为NaCl溶液,呈中性,若M为镁,电池总的化学方程式为2Mg+02+2H2O=2Mg(OH)2;故C错误;
D.若M为铁,则负极Fe失去电子生成二价铁离子,则负极的电极反应式为Fe-2e-=Fe2+,故D正确;
故选D.
点评:本题考查了金属燃料电池,本题难度不大,注意电极反应式的书写,结合电解质溶液分析.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

