��Ŀ����
��15�֣�
��֪A��B��C��D��E��F�������ڱ���ǰ�����ڵ�Ԫ�أ����ǵĺ˵����A��B��C��D��E��F������Aԭ�Ӻ���������δ�ɶԵ��ӣ�������B2E�ľ���Ϊ���Ӿ��壬Eԭ�Ӻ����M����ֻ�����ԳɶԵ��ӣ�CԪ���ǵؿ��к�����ߵĽ���Ԫ�أ�D���ʵľ���������ͬ���ڵĵ�����û����ͬ�ģ�Fԭ�Ӻ���������������B��ͬ�����������Ӿ������������������Ϣ���ش��������⣺������ʱ��A��B��C��D��E��F������Ӧ��Ԫ�ط��ű�ʾ��
��1��A��B��C��D�ĵ�һ��������С�����˳��Ϊ ��(��Ԫ�ط��ű�ʾ)
��2��B���Ȼ�����۵��D���Ȼ�����۵� �����ͣ���
������ ��
��3��A������������Ӧ��ˮ���������������ԭ�Ӳ�ȡ �ӻ���E�������������ӵĿռ乹���� ��
��4��F�ĺ�������Ų�ʽ�� ��F�ĸ�������A�ļ��⻯���γɵ������ӵĻ�ѧʽΪ .
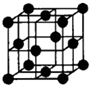
��5��A��F�γ�ij�ֻ�����ľ����ṹ��ͼ��ʾ������A��-3�ۣ������仯ѧʽΪ ����ÿ�������ʾ1��ԭ�ӣ�
��6��A��C�γɵĻ�������и߷е��Ӳ�ȣ���һ���������ǽ������ϣ����仯ѧʽΪ ���侧���������Ļ�ѧ������Ϊ ��
��15�֣�
��1��Na��Al��Si��N��2�֣�
��2���ߣ�1�֣���NaClΪ���Ӿ����SiCl4Ϊ���Ӿ��壨1�֣�
��3��sp2��2�֣���ƽ���������Σ�2�֣�
��4��1s22s22p63s23p63d104s1����[Ar] 3d104s1����2�֣� [Cu(NH3)4]2+��1�֣�
��5��Cu3N ��2�֣�
��6��AlN��1�֣������ۼ���1�֣�
����:

| A��Fe��Cu��Al��Ag | B��Al��Cu��Fe��Ag | C��Cu��Ag��Al��Fe | D��Ag��Al��Cu��Fe |

 ��֪A��B��C��D��E������������ͼ��ʾ��ת����ϵ�����ַ�Ӧ�P��Ӧ����δ�г���������ʱ��Ҫ�������������裩�������������о�����AԪ�أ�
��֪A��B��C��D��E������������ͼ��ʾ��ת����ϵ�����ַ�Ӧ�P��Ӧ����δ�г���������ʱ��Ҫ�������������裩�������������о�����AԪ�أ� ����ͨ������£���A��BΪ���ӣ�C��EΪ�����ӣ�DΪ�����ӣ����Ƕ�����10�����ӣ�B����A�����õ����ʿɵ����C��D��A��B��E��������Ӧ��ɵ�C��һ�ְ�ɫ��������ش�
����ͨ������£���A��BΪ���ӣ�C��EΪ�����ӣ�DΪ�����ӣ����Ƕ�����10�����ӣ�B����A�����õ����ʿɵ����C��D��A��B��E��������Ӧ��ɵ�C��һ�ְ�ɫ��������ش�