题目内容
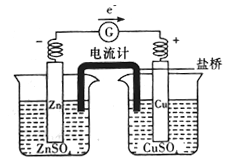
【题目】下列选用的仪器和药品能达到实验目的的是
A | B | C | D |
|
|
|
|
准确量取一定体积KMnO4标准溶液 | 探究不同催化剂对反应速率的影响 | 观察Fe(OH)2的颜色 | 证明非金属性S>Si |
A. A B. B C. C D. D
【答案】C
【解析】A、这是碱式滴定管,盛放碱性溶液,酸性高锰酸钾溶液应盛放在酸式滴定管,故A错误;B、研究某一种因素对化学反应速率的影响,要求其他条件不变,故B错误;C、苯防止空气中氧气进入溶液中,可以长时间观察Fe(OH)2的颜色,故C正确;D、SO2溶于水生成H2SO3,其中S显+4价,不是最高价,溶液变浑浊,说明亚硫酸的酸性强于硅酸,但不能说明S的非金属性大于Si,通过酸性的强弱比较非金属性,应是最高价氧化物对应的水化物,故D错误。

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
【题目】向下图装置中缓慢地通入气体X,若关闭活塞,则品红溶液无变化,而澄清石灰水变浑浊;若打开活塞,则品红溶液褪色,加热后乂恢复红色。据此判断气体X和洗气瓶内溶液Y分别可能是
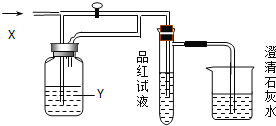
A | B | C | D | |
X | SO2 | H2S | CO2 | Cl2 |
Y | 饱和NaHCO3 | 浓硫酸 | Na2SO3 | NaHCO3 |
A. A B. B C. C D. D