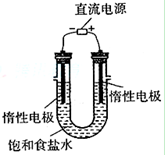
题目内容
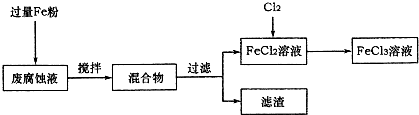
某同学为将含有少量杂质铜的氯化铁提纯,拟定以下实验步骤:
①把样品加蒸馏水溶解;
②过滤除去杂质;
③把滤液加热蒸干得到FeCl3晶体.
(1)你认为此方案是否科学,试用化学方程式和简要文字表达其理由.
答____________________.
(2)请你设计提纯氯化铁的方案(只要求写出提纯步骤,最多只允许6步完成).
答____________________.
解析:
|
(1)不科学;加水后:2FeCl3+Cu=CuCl2+2FeCl2,过滤不能除去CuCl2;在溶液蒸干过程中,FeCl3+3H2O (2)①加蒸馏水溶解②加过量Fe粉③过滤除去Cu和过量的Fe④通入适量氯气⑤通入HCl气体⑥蒸发、浓缩、结晶得到FeCl3晶体. |

 新课标快乐提优暑假作业陕西旅游出版社系列答案
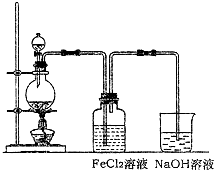
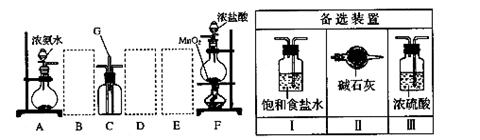
新课标快乐提优暑假作业陕西旅游出版社系列答案(14分)某课外活动小组用如图所示的实验装置探究氯气与氨气之间的反应。其中A、F为氨气和氯气的发生装置,C为纯净、干燥的氯气与氨气反应的装置。![]()
|
![]()
![]() 请回答下列问题:
请回答下列问题:
![]() (1)装置F中发生反应的离子方程式是 。
(1)装置F中发生反应的离子方程式是 。
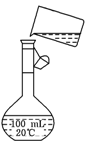
![]() (2)装置A中的烧瓶内固体可选用 (选填以下选项的代号)。
(2)装置A中的烧瓶内固体可选用 (选填以下选项的代号)。
![]() A.碱石灰 B.浓硫酸 C.生石灰 D.五氧化二磷 E.烧碱
A.碱石灰 B.浓硫酸 C.生石灰 D.五氧化二磷 E.烧碱
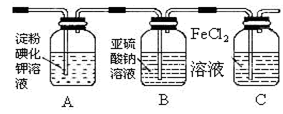
![]() (3)虚线框内应添加必要的除杂装置,请从右图的备选装置中选择,并将编号填入下列B 、D 、E 。
(3)虚线框内应添加必要的除杂装置,请从右图的备选装置中选择,并将编号填入下列B 、D 、E 。
![]() (4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为: ;装置C内出现浓厚的白烟并在容器内壁凝结,某同学设计一个实验方案鉴定该固体就是氯化铵:
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为: ;装置C内出现浓厚的白烟并在容器内壁凝结,某同学设计一个实验方案鉴定该固体就是氯化铵:
![]() 步骤①:取固体样品加少量水溶解,分装于两支试管中。向其中一支试管中加入浓NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口附近,红色石蕊试纸变蓝,证明该固体中含有
步骤①:取固体样品加少量水溶解,分装于两支试管中。向其中一支试管中加入浓NaOH溶液,加热,将湿润的红色石蕊试纸放在试管口附近,红色石蕊试纸变蓝,证明该固体中含有
![]() 步骤②:
步骤②:
![]() (5)若从装置C和G处逸出的尾气中含有N2和少量C12,应如何处理?(用离子方程式表示) 。
(5)若从装置C和G处逸出的尾气中含有N2和少量C12,应如何处理?(用离子方程式表示) 。