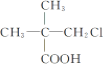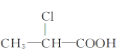题目内容
【题目】已知工业上常用“有效氢含量”衡量含氢还原剂的还原能力,其定义为 :每克含氢还原剂的还原能力相当于多少克H2的还原能力。硼氢化钠(NaBH4)是一种极强的含氢还原剂,下列有关说法正确的是
A.NaBH4作还原剂时 ,其中的硼元素被氧化
B.NaBH4 的“有效氢含量”约为0.21
C.反应8Au3+ +BH![]() +OH-→ 8Au+BO
+OH-→ 8Au+BO![]() +H2O中水的化学计量数为16
+H2O中水的化学计量数为16
D.NaBH4遇水产生大量的氧气可作供氧剂
【答案】B
【解析】
A. NaBH4中B元素的化合价为+3,H元素的化合价为-1,NaBH4作还原剂时 ,其中的硼元素的化合价不变,被氧化的是氢元素,A说法不正确;
B. 1mol NaBH4作还原剂时,H元素由-1价升高到+1价,可以失去8mol电子,相当于4mol H2 ,NaBH4 的“有效氢含量”为![]() 0.21,B说法正确;
0.21,B说法正确;
C. 配平后可得8Au3+ +3BH![]() +24OH- = 8Au+3BO
+24OH- = 8Au+3BO![]() +18H2O,则水的化学计量数为18,C说法不正确;
+18H2O,则水的化学计量数为18,C说法不正确;
D. NaBH4是一种极强还原剂,其与水产生氢气,不可能用作供氧剂,D说法不正确。
本题选B。

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目