题目内容
物质在水中可能存在电离平衡、盐的水解平衡等,它们都可看作化学平衡。请根据所学的知识回答:
(1)A为0.1mol?L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为 。
(2)B为0.1 mol?L-1NaHCO3溶液,在NaHCO3溶液中存在的各种平衡体系为(分别用离子方程式表示): ;实验测得NaHCO3溶液的pH>7,请分析NaHCO3溶液显碱性的原因: 。
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入 ,目的是
;将B和C溶液混合后,反应的离子方程式为 。
(1)c(NH4+)>c(SO42-)> c (H+)>c(OH-)
(2)HCO3-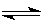 H++CO32-、HCO3-+H2O
H++CO32-、HCO3-+H2O H2CO3+OH- 、H2O
H2CO3+OH- 、H2O H++OH-
H++OH-
HCO3-的水解程度大于其电离程度,溶液中c(OH-)> c (H+),故溶液显碱性。
(3)盐酸 抑制Fe3+水解 Fe3++ 3HCO3- Fe(OH)3↓ +3CO2↑
Fe(OH)3↓ +3CO2↑
解析

 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||