ΧβΡΩΡΎ»ί
ΓΨΧβΡΩΓΩΒΣΓΔΝΉΦΑΤδΜ·ΚœΈο‘ΎΙΛ≈©“Β…ζ≤ζ÷–ΕΦ”–÷Ί“ΣΉς”ΟΓΘ
Θ®1Θ©ΜυΧ§ΝΉ‘≠Ή”ΦέΒγΉ”≈≈≤ΦΒΡΙλΒά±μ Ψ ΫΈΣ___________ΓΘ
Θ®2Θ©‘ΣΥΊBΓΔNΓΔOΒΡΒΎ“ΜΒγάκΡή”…¥σΒΫ–ΓΒΡΥ≥–ρΈΣ___________ΓΘ
Θ®3Θ© ≥ΤΖΧμΦ”ΦΝNaNO2÷–NO2-÷––Ρ‘≠Ή”ΒΡ‘”Μ·άύ–Ά «_____Θ§”κNO2-ΜΞΈΣΒ»ΒγΉ”ΧεΒΡΖ÷Ή”ΒΡΜ·―ß ΫΈΣ___________ΓΘ(–¥1÷÷)ΓΘ
Θ®4Θ©N2H4 «ΜπΦΐΒΡ»ΦΝœΘ§”κ―θΤχΒΡœύΕ‘Ζ÷Ή”÷ ΝΩœύΆ§Θ§Υϋ‘Ύ≥ΘΈ¬≥Θ―Ιœ¬ «“ΚΧ§Θ§Εχ―θΤχ «ΤχΧ§Θ§‘λ≥…’β÷÷≤ν“λΒΡ÷ς“Σ‘≠“ρ «____________ΓΘ
Θ®5Θ©ΝΉΜ·≈π «“Μ÷÷ΡΆΡΞΆΩΝœΘ§ΥϋΩ…”ΟΉςΫπ τΒΡ±μΟφ±ΘΜΛ≤ψΓΘΝΉΜ·≈πΩ…”…»ΐδεΜ·≈πΚΆ»ΐδεΜ·ΝΉ”ΎΗΏΈ¬œ¬‘Ύ«βΤχ÷–Ζ¥”ΠΚœ≥…ΓΘ
ΔΌ»ΐδεΜ·ΝΉΖ÷Ή”ΒΡΩ’ΦδΙΙ–Ά «_________Θ§»ΐδεΜ·≈πΦϋΫ« «___________ΓΘ
ΔΎΝΉΜ·≈πΨßΧεΨßΑϊ»γΆΦΥυ Ψ:Τδ÷– Β–Ρ«ρΈΣΝΉ‘≠Ή”Θ§‘Ύ“ΜΗωΨßΑϊ÷–ΝΉ‘≠Ή”Ω’ΦδΕ―ΜΐΖΫ ΫΈΣ________Θ§ΝΉ‘≠Ή”ΒΡ≈δΈΜ ΐΈΣ___________Θ§ΗΟΫαΙΙ÷–”–“ΜΗω≈δΈΜΦϋΘ§ΧαΙ©Ω’ΙλΒάΒΡ‘≠Ή” «___________ΓΘΦΚ÷ΣΨßΑϊ±Ώ≥ΛapmΘ§ΑΔΖϋΦ”Β¬¬ό≥Θ ΐΈΣNAΓΘ‘ρΝΉΜ·≈πΨßΧεΒΡΟήΕ»ΈΣ___________g/cm3ΓΘ

ΔέΝΉΜ·≈πΨßΑϊ―ΊΉ≈ΧεΕ‘Ϋ«œΏΖΫœρΒΡΆΕ”Α(ΆΦ÷––ιœΏ‘≤»Π±μ ΨP‘≠Ή”ΒΡΆΕ”Α)Θ§”Ο ΒœΏ‘≤»ΠΜ≠≥ωB‘≠Ή”ΒΡΆΕ”ΑΈΜ÷Ο(ΉΔ“β‘≠Ή”ΧεΜΐΒΡœύΕ‘¥σ–Γ)ΓΘ______
ΓΨ¥πΑΗΓΩ N>O>B sp2‘”Μ· SO2ΓΔO3 N2H4Ζ÷Ή”Φδ¥φ‘Ύ«βΦϋΘ§O2Ζ÷Ή”Φδ÷Μ”–ΖΕΒ¬ΜΣΝΠΘ§«βΦϋ±»ΖΕΒ¬ΜΣΝΠ«Ω »ΐΫ«ΉΕ–Έ 120Γψ Οφ–ΡΝΔΖΫΉνΟήΕ―Μΐ 4 B
N>O>B sp2‘”Μ· SO2ΓΔO3 N2H4Ζ÷Ή”Φδ¥φ‘Ύ«βΦϋΘ§O2Ζ÷Ή”Φδ÷Μ”–ΖΕΒ¬ΜΣΝΠΘ§«βΦϋ±»ΖΕΒ¬ΜΣΝΠ«Ω »ΐΫ«ΉΕ–Έ 120Γψ Οφ–ΡΝΔΖΫΉνΟήΕ―Μΐ 4 B ![]()
 Μρ
Μρ
ΓΨΫβΈωΓΩ
(1)PΈΣ15Κ≈‘ΣΥΊΘ§ΜυΧ§ΝΉ‘≠Ή”ΦέΒγΉ”≈≈≤ΦΒΡΙλΒά±μ Ψ ΫΈΣ Θ§Ι ¥πΑΗΈΣΘΚ
Θ§Ι ¥πΑΗΈΣΘΚ ΘΜ
ΘΜ
(2)Ά§“Μ÷ήΤΎΘ§¥”ΉσΒΫ”“Θ§‘ΣΥΊΒΡΒΎ“ΜΒγάκΡή÷πΫΞ‘ω¥σΘ§ΒΪNΒΡ2pΈΣΑκ≥δ¬ζΉ¥Χ§Θ§ΨυΈΣΈ»Ε®Θ§ΒΎ“ΜΒγάκΡή¥σ”ΎOΘ§ΒΎ“ΜΒγάκΡή”…¥σΒΫ–ΓΒΡΥ≥–ρΈΣN>O>BΘ§Ι ¥πΑΗΈΣΘΚN>O>BΘΜ
(3) ≥ΤΖΧμΦ”ΦΝNaNO2÷–NO2-÷––Ρ‘≠Ή”N”κ2Ηω‘≠Ή”œύΝ§Θ§Ι¬Ε‘ΒγΉ”Ε‘ ΐ=![]() (5+1-2ΓΝ2)=1Θ§≤…”Οsp2Θ§”κNO2-ΜΞΈΣΒ»ΒγΉ”ΧεΒΡΖ÷Ή””–SO2ΓΔO3Θ§Ι ¥πΑΗΈΣΘΚsp2‘”Μ·ΘΜSO2ΓΔO3ΘΜ
(5+1-2ΓΝ2)=1Θ§≤…”Οsp2Θ§”κNO2-ΜΞΈΣΒ»ΒγΉ”ΧεΒΡΖ÷Ή””–SO2ΓΔO3Θ§Ι ¥πΑΗΈΣΘΚsp2‘”Μ·ΘΜSO2ΓΔO3ΘΜ
(4)N2H4Ζ÷Ή”Φδ¥φ‘Ύ«βΦϋΘ§O2Ζ÷Ή”Φδ÷Μ”–ΖΕΒ¬ΜΣΝΠΘ§«βΦϋ±»ΖΕΒ¬ΜΣΝΠ«ΩΘ§ΒΦ÷¬‘Ύ≥ΘΈ¬≥Θ―Ιœ¬N2H4 «“ΚΧ§Θ§Εχ―θΤχ «ΤχΧ§Θ§Ι ¥πΑΗΈΣΘΚN2H4Ζ÷Ή”Φδ¥φ‘Ύ«βΦϋΘ§O2Ζ÷Ή”Φδ÷Μ”–ΖΕΒ¬ΜΣΝΠΘ§«βΦϋ±»ΖΕΒ¬ΜΣΝΠ«ΩΘΜ
(5)ΔΌ»ΐδεΜ·ΝΉΖ÷Ή”÷–ΝΉ‘≠Ή”ΒΡΦέ≤ψΒγΉ”Ε‘ ΐΈΣ![]() =4Θ§P‘≠Ή”Α¥sp3ΖΫ Ϋ‘”Μ·Θ§”–“ΜΕ‘Ι¬ΒγΉ”Ε‘Θ§Υυ“‘Ζ÷Ή”Ω’ΦδΙΙ–ΆΈΣ»ΐΫ«ΉΕ–ΈΘ§»ΐδεΜ·≈πΖ÷Ή”÷–≈π‘≠Ή”ΒΡΦέ≤ψΒγΉ”Ε‘ ΐΈΣ
=4Θ§P‘≠Ή”Α¥sp3ΖΫ Ϋ‘”Μ·Θ§”–“ΜΕ‘Ι¬ΒγΉ”Ε‘Θ§Υυ“‘Ζ÷Ή”Ω’ΦδΙΙ–ΆΈΣ»ΐΫ«ΉΕ–ΈΘ§»ΐδεΜ·≈πΖ÷Ή”÷–≈π‘≠Ή”ΒΡΦέ≤ψΒγΉ”Ε‘ ΐΈΣ![]() =3Θ§B‘≠Ή”Α¥sp2ΖΫ Ϋ‘”Μ·Θ§ΟΜ”–Ι¬ΒγΉ”Ε‘Θ§Υυ“‘Ζ÷Ή”Ω’ΦδΙΙ–ΆΈΣΤΫΟφ»ΐΫ«–ΈΘ§ΫαΙΙ ΫΈΣ
=3Θ§B‘≠Ή”Α¥sp2ΖΫ Ϋ‘”Μ·Θ§ΟΜ”–Ι¬ΒγΉ”Ε‘Θ§Υυ“‘Ζ÷Ή”Ω’ΦδΙΙ–ΆΈΣΤΫΟφ»ΐΫ«–ΈΘ§ΫαΙΙ ΫΈΣ![]() Θ§ΦϋΫ« «120ΓψΘ§Ι ¥πΑΗΈΣΘΚ»ΐΫ«ΉΕ–ΈΘΜ120ΓψΘΜ
Θ§ΦϋΫ« «120ΓψΘ§Ι ¥πΑΗΈΣΘΚ»ΐΫ«ΉΕ–ΈΘΜ120ΓψΘΜ
ΔΎΗυΨίΝΉΜ·≈πΨßΧεΨßΑϊΫαΙΙΆΦΘ§‘Ύ“ΜΗωΨßΑϊ÷–ΝΉ‘≠Ή”Ω’ΦδΕ―ΜΐΖΫ ΫΈΣΟφ–ΡΝΔΖΫΉνΟήΕ―ΜΐΘ§ΨßΑϊ÷–ΝΉ‘≠Ή”ΚΆ≈π‘≠Ή”ΕΦ «4ΗωΘ§BΒΡ≈δΈΜ ΐΈΣ4Θ§‘ρPΒΡ≈δΈΜ ΐ“≤ΈΣ4Θ§ΗΟΫαΙΙ÷–”–“ΜΗω≈δΈΜΦϋΘ§B‘≠Ή”ΉνΆβ≤ψ”–3ΗωΒγΉ”Θ§ΧαΙ©Ω’ΙλΒάΒΡ‘≠Ή” «BΓΘΨßΑϊ÷–ΝΉ‘≠Ή”ΚΆ≈π‘≠Ή”ΕΦ «4ΗωΘ§‘ρΨßΑϊΒΡΟήΕ»= =
=![]() g/cm3Θ§Ι ¥πΑΗΈΣΘΚΟφ–ΡΝΔΖΫΉνΟήΕ―ΜΐΘΜ4ΘΜBΘΜ
g/cm3Θ§Ι ¥πΑΗΈΣΘΚΟφ–ΡΝΔΖΫΉνΟήΕ―ΜΐΘΜ4ΘΜBΘΜ![]() ΘΜ
ΘΜ
ΔέΗυΨίΝΉΜ·≈πΒΡΨßΑϊΫαΙΙΆΦΘ§―ΊΉ≈ΧεΕ‘Ϋ«œΏΖΫœρΒΡΆΕ”ΑΈΣ (ΆΦ÷––ιœΏ‘≤»Π±μ ΨP‘≠Ή”ΒΡΆΕ”ΑΘ§ ΒœΏ‘≤»ΠΈΣB‘≠Ή”ΒΡΆΕ”ΑΘ§Τδ÷–P‘≠Ή”ΑκΨΕ±»B¥σΘ§Ι ¥πΑΗΈΣΘΚ
(ΆΦ÷––ιœΏ‘≤»Π±μ ΨP‘≠Ή”ΒΡΆΕ”ΑΘ§ ΒœΏ‘≤»ΠΈΣB‘≠Ή”ΒΡΆΕ”ΑΘ§Τδ÷–P‘≠Ή”ΑκΨΕ±»B¥σΘ§Ι ¥πΑΗΈΣΘΚ ΓΘ
ΓΘ

 ‘ΡΕΝΩλ≥ΒœΒΝ–¥πΑΗ
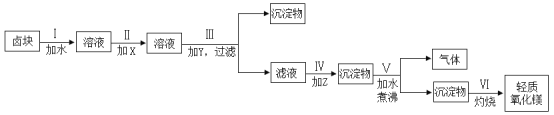
‘ΡΕΝΩλ≥ΒœΒΝ–¥πΑΗΓΨΧβΡΩΓΩ¬±ΩιΒΡ÷ς“Σ≥…Ζ÷ «MgCl2Θ§¥ΥΆβΜΙΚ§”–Fe3+ΓΔFe2+ΚΆMn2+Β»άκΉ”ΓΘ»τ“‘ΥϋΈΣ‘≠ΝœΑ¥œ¬ΆΦΥυ ΨΙΛ“’Νς≥ΧΫχ––…ζ≤ζΘ§Ω…÷ΤΒΟ«α÷ ―θΜ·ΟΨΓΘ
“―÷Σ1ΘΚ…ζ≥…«β―θΜ·Έο≥ΝΒμΒΡpH
Έο÷ | ΩΣ Φ≥ΝΒμ | ≥ΝΒμΆξ»Ϊ |
Fe(OH)2 | 7.6 | 9.6 |
Fe(OH)3 | 2.7 | 3.7 |
Mn(OH)2 | 8.3 | 9.8 |
Mg(OH)2 | 9.6 | 11.1 |
“―÷Σ2ΘΚΦΗ÷÷Ρ―»ήΒγΫβ÷ ΒΡ»ήΫβΕ»Θ®20ΓφΘ©
Έο÷ | »ήΫβΕ»/g |
Fe(OH)2 | 5.2ΓΝ10-5 |
Fe(OH)3 | 3ΓΝ10-9 |
MgCO3 | 3.9ΓΝ10-2 |
Mg(OH)2 | 9ΓΝ10-4 |
Θ®“―÷ΣΘΚFe2+«β―θΜ·Έο≥ –θΉ¥Θ§≤Μ“Ή¥”»ή“Κ÷–≥ΐ»ΞΘ©
«κΜΊ¥πΘΚ
Θ®1Θ©≤Ϋ÷ηΔρ÷–Φ”»κΒΡ ‘ΦΝXΈΣΤ·“ΚΘ®Κ§25.2%NaClOΘ©ΓΘ
ΔΌ”Ο≤ΘΝßΑτ’Κ»ΓΤ·“ΚΒΈ‘ΎpH ‘÷Ϋ…œΘ§pH ‘÷Ϋœ»±δάΕΘ§ΚσΆ …ΪΓΘΥΒΟςΤ·“ΚΨΏ”–ΒΡ–‘÷ «________ΓΘ
ΔΎ”ΟΜ·―ß”Ο”ο±μ ΨNaClO»ή“Κ ΙpH ‘÷Ϋ±δάΕΒΡ‘≠“ρ_________ΓΘ
Δέ≤Ϋ÷ηΔρ÷–Τ·“ΚΒΡ÷ς“ΣΉς”Ο «__________ΓΘ
Δή»τ”ΟH2O2¥ζΧφΤ·“ΚΘ§ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ_________ΓΘ
Θ®2Θ©≤Ϋ÷ηΔσ÷–Φ”»κΒΡ ‘ΦΝYΈΣNaOHΘ§”ΠΫΪ»ή“ΚΒΡpHΒςΫΎΈΣ______Θ§ΡΩΒΡ «_______ΓΘ
Θ®3Θ©≤Ϋ÷ηΔτ÷–Φ”»κΒΡ ‘ΦΝZΈΣNa2CO3Θ§ΖΔ…ζΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ_______ΓΘ
Θ®4Θ©ΫαΚœΜ·―ß”Ο”οΘ§”Π”ΟΜ·―ßΤΫΚβ“ΤΕ·‘≠άμΫβ Ά≤Ϋ÷ηΔθ÷–Ζ¥”ΠΖΔ…ζΒΡ‘≠“ρ_______ΓΘ