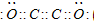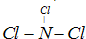题目内容
现有A、B、C、D,4种元素,前3种元素的离子都和氖原子具有相同的核外电子排布.A元素没有正化合价;B的氢化物分子式为H2B,0.2 mol的C单质能从酸中置换出2.24 L H2(标准状况).D的原子核中没有中子.
(1)根据以上条件,推断A、B、C、D的元素名称:A.________,B.________,C.________,D.________.
(2)用电子式表示C与A、C与B、B与D相互结合成的化合物,指出其化合物的类型及化学键类型:
C+A:电子式________,化合物类型:________,化学键类型:________.
C+B:电子式________,化合物类型:________,化学键类型:________.
B+D:电子式________,化合物类型:________,化学键类型:________.
(3)写出C与B所形成的化合物与D与B所形成的化合物反应的离子方程式:________.
答案:

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C、D形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态.
现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C、D形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态.