��Ŀ����
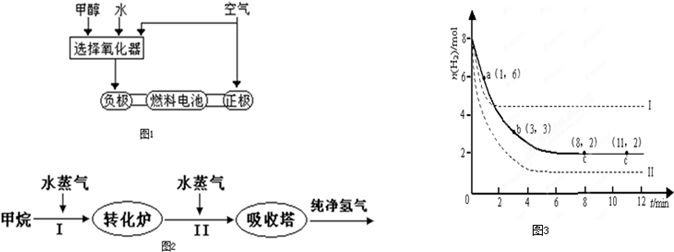
(9��)��2L�ܱ������ڣ�800��ʱ��Ӧ��2NO(g)+O2(g) 2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
2NO2(g)��ϵ�У�n(NO)��ʱ��ı仯�����
| ʱ��(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010. | 0.008 | 0.007 | 0. 007 | 0.007 |
����ͼ�б�ʾNO2��Ũ�ȱ仯������ ��
��O2��ʾ��0~2s�ڸ÷�Ӧ��ƽ������v= ��
����˵���÷�Ӧ�Ѵﵽƽ��״̬���� ��
a��v (NO2)="2" v (O2) b��������ѹǿ���ֲ���
c��v�� (NO)="2" v�� (O2) d�������ڻ��������ܶȱ��ֲ���
e.����������ɫ���ֲ���
��1��65% ��2�֣� ��2��b ��2�֣�
��3��0.0015mol��L-1��S-1 ��2�֣� ��4��b��c��e ��3�֣�
����

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�(14��) �о�NO2��SO2 ��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
(1)���÷�Ӧ6NO2��8NH3  7N2��12H2O�ɴ���NO2����ת��3.6mol����ʱ�����ɵ�N2�ڱ�״������
L��
7N2��12H2O�ɴ���NO2����ת��3.6mol����ʱ�����ɵ�N2�ڱ�״������
L��
(2)��֪����Ӧ1��2SO2(g)+O2(g) 2SO3(g) ��H = ��196.6 kJ��mol-1
2SO3(g) ��H = ��196.6 kJ��mol-1
��Ӧ2��NO2(g)+SO2(g) SO3(g)+NO(g) ��H = ��41.8kJ��mol-1
SO3(g)+NO(g) ��H = ��41.8kJ��mol-1
��3��2NO(g)+O2(g) 2NO2(g)�� ��H
= _________ kJ��mol-1
2NO2(g)�� ��H
= _________ kJ��mol-1
(3) һ�������£���2molNO��2molO2���ں����ܱ������з���������Ӧ3�����и�����˵����Ӧ�ﵽƽ��״̬���� ��
a����ϵѹǿ���ֲ��� b�����������ɫ���ֲ���
c��NO��O2�����ʵ���֮�ȱ��ֲ��� d��ÿ����1 molO2ͬʱ����2 molNO2
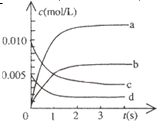
(4)CO�����ںϳɼ״���һ���¶��£������Ϊ2L���ܱ������м���CO��H2��������ӦCO��g��+2H2��g�� CH3OH��g������ƽ����ø����Ũ�����£�
CH3OH��g������ƽ����ø����Ũ�����£�
|
���� |
CO |
H2 |
CH3OH |
|
Ũ��(mol•L��1) |
0.9 |
1.0 |
0.6 |
�ٻ�������ƽ����Է�������__________________________��
����ʽ������ƽ�ⳣ��K=__________________________��
�������������ѹ��Ϊ1L,�������㣬Ԥ����ƽ����c(H2)��ȡֵ��Χ��__________��
��������������䣬�ٳ���0.6molCO��0.4molCH3OH,��ʱv��___v��(�>������<����=��)��