题目内容
 已知A是由两种元素组成的常见化合物,A在如图转化关系 (某些转化关系中的产物已略去)中都是中学化学常见的物质,物质C、D、F是单质,①是工业上一个重要反应,I常用于漂白.③历史上著名制碱反应,K为白色固体.
已知A是由两种元素组成的常见化合物,A在如图转化关系 (某些转化关系中的产物已略去)中都是中学化学常见的物质,物质C、D、F是单质,①是工业上一个重要反应,I常用于漂白.③历史上著名制碱反应,K为白色固体.请回答下列问题:
(1)写出下列物质化学式:B
NaOH
NaOH
INaClO
NaClO
FNa
Na
(2)写出反应①的化学方程式:
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
| ||
2NaCl+2H2O
2NaOH+H2↑+Cl2↑
写出A电解化学方程式:
| ||
2NaCl
2Na+Cl2↑
| ||
2NaCl
2Na+Cl2↑
| ||
(3)写出G→K的化学方程式
2NaHCO3
Na2CO3+CO2↑+H2O
| ||
2NaHCO3
Na2CO3+CO2↑+H2O
.
| ||
分析:本题中E常温下最常见的液体,则应为水,H是极易溶于水的酸性气体溶于水是一种的强酸,则H应为HCl,由C、D两种单质生成,则C、D分别为H2和Cl2,结合①是工业上一个重要反应可判断A是NaCl,①的反应为电解饱和食盐水,则可知B为NaOH,反应②为电解熔融的NaCl,且F为单质,应为Na,③是历史上著名制碱反应,即侯氏制碱法,生成的G为NaHCO3,K为Na2CO3,I常用于漂白,由Cl2和NaOH反应生成,应为NaClO,结合物质的有关性质可完成以下各题.
解答:解:(1)E常温下最常见的液体,则应为水,H是极易溶于水的酸性气体溶于水是一种的强酸,则H应为HCl,由C、D两种单质生成,则C、D分别为H2和Cl2,结合①是工业上一个重要反应可判断A是NaCl,①的反应为电解饱和食盐水,则可知B为NaOH,反应②为电解熔融的NaCl,且F为单质,应为Na,I常用于漂白,由Cl2和NaOH反应生成,应为NaClO,
故答案为:NaOH;NaClO;Na;
(2)①反应为氯碱工业,即电解饱和食盐水,应②为电解熔融的NaCl,根据电解原理可知电解方程式,故
答案为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑;2NaCl
2Na+Cl2↑;
(3)由以上分析G为NaHCO3,K为Na2CO3,NaHCO3分解生成Na2CO3,根据物质的性质可写出化学方程式,
故答案为:2NaHCO3
Na2CO3+CO2↑+H2O.
故答案为:NaOH;NaClO;Na;
(2)①反应为氯碱工业,即电解饱和食盐水,应②为电解熔融的NaCl,根据电解原理可知电解方程式,故
答案为:2NaCl+2H2O
| ||
| ||
(3)由以上分析G为NaHCO3,K为Na2CO3,NaHCO3分解生成Na2CO3,根据物质的性质可写出化学方程式,
故答案为:2NaHCO3
| ||
点评:本题考查无机物的推断和元素化合物知识,做题时注意找出题目的突破口是做题的关键,注意积累基础知识.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目

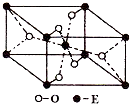 已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D元素是地壳中含量最多的元素.E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同.
已知A、B、C、D、E五种元素的原子序数依次递增,A、B、C、D位于前三周期.A位于周期表的s区,其原子中电子层数和未成对电子数相同;B的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子总数相同;D元素是地壳中含量最多的元素.E有“生物金属”之称,E4+离子和氩原子的核外电子排布相同.







