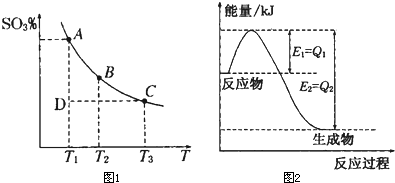
题目内容
运用化学反应原理研究氮、氧等单质及其化合物的反应有重要意义.(1)合成氨反应N2(g)+3H2(g)?2NH3(g),在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”、“向右”或“不”);使用催化剂使反应的△H (填“增大”、“减小”或“不改变”).
(2)在25℃下,向浓度均为0.1mol?L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,沉淀会分步析出.
首先生成沉淀的离子方程式为 氨水过量后,生成的沉淀会部分溶解,写出溶解沉淀的离子方程式 .
(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20)
(3)在25℃下,将a mol?L-1的氨水与0.01mol?L-1的盐酸等体积混合,反应后溶液中
c(NH4+)=c(Cl-).则溶液显 性(填“酸”、“碱”或“中”),请用含a的代数式表示NH3?H2O的电离常数Kb= .
(4)在一个固定容积为5L的密闭容器中充入0.20mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO30.18mol,则v(o2)= mol.L-1.min-1:若继续通入0.20mol SO2和0.10mol O2,再次达到平衡后,n(SO3)的取值范围为 .
【答案】分析:(1)恒温恒压条件下向平衡体系中通入氩气,体积增大,等效为降低压强,平衡向体积增大的方向移动;
反应热只与始态与状态有关,催化剂改变平衡建立的途径,不影响始态与终态,反应热不变;
(2)Mg(OH)2、Cu(OH)2的结构类型相同,溶度积越小,溶解度越小,加入相同的浓度的氨水,最先析出;氨水过量,氢氧化铜与氨水反应生成四氨合铜络离子;
(3)根据电荷守恒判断溶液中氢离子与氢氧根离子浓度的相对大小,进而判断溶液的酸碱性;
溶液中存在平衡NH3.H2O?NH4++OH-,根据溶液的pH值计算溶液中c(OH-),根据氯离子浓度计算c(NH4+),利用物料守恒计算溶液中c(NH3.H2O),代入NH3?H2O的电离常数表达式计算;
(4)根据平衡时三氧化硫的物质的量计算氧气的物质的量变化量,根据v=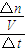 计算v(O2);
计算v(O2);
再加入0.20mol SO2和0.10mol O2,等效为开始加入0.40mol SO2和0.20mol O2,等效为增大压强,平衡向正反应移动,二氧化硫的转化率增大,据此确定n(SO3)的极小值,反应为可逆反应,假定完全反应确定n(SO3)的极大值.
解答:解:(1)恒温恒压条件下向平衡体系中通入氩气,体积增大,等效为降低压强,平衡向体积增大的方向移动,该反应正反应是体积减小的反应,故平衡向左移动.
反应热只与始态与状态有关,催化剂改变平衡建立的途径,不影响始态与终态,反应热不变,
故答案为:作,不改变;
(2)Mg(OH)2、Cu(OH)2的结构类型相同,Cu(OH)2溶度积更小,溶解度越小,加入相同的浓度的氨水,Cu(OH)2最先析出,反应离子方程式为:Cu2++2NH3.H2O=Cu(OH)2↓+2NH4+,氨水过量,氢氧化铜与氨水反应生成四氨合铜络离子,离子方程式为:Cu(OH)2+4NH3.H2O=[Cu(NH3)4]2++2OH-+4H2O,
故答案为:Cu2++2NH3.H2O=Cu(OH)2↓+2NH4+,Cu(OH)2+4NH3.H2O=[Cu(NH3)4]2++2OH-+4H2O;
(3)根据电荷守恒有c(NH4+)+c(H+)=c(Cl-)+c(OH-),由于c(NH4+)=c(Cl-),故c(H+)=c(OH-),溶液呈中性,故溶液中c(OH-)=10-7mol/L,溶液中c(NH4+)=c(Cl-)= ×0.01mol?L-1=0.005mol?L-1,故混合后溶液中c(NH3.H2O)=
×0.01mol?L-1=0.005mol?L-1,故混合后溶液中c(NH3.H2O)= ×amol?L-1-0.005mol?L-1=(0.5a-0.005)mol/L,NH3?H2O的电离常数Kb=
×amol?L-1-0.005mol?L-1=(0.5a-0.005)mol/L,NH3?H2O的电离常数Kb=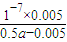 =
=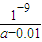 ,
,
故答案为:中,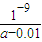 ;
;
(4)平衡时三氧化硫的物质的量为0.18mol,由方程式可知,氧气的物质的量变化量为0.18mol× =0.09mol,所以v(O2)=
=0.09mol,所以v(O2)= =0.036mol/(L?min),
=0.036mol/(L?min),
再加入0.20mol SO2和0.10mol O2,等效为开始加入0.40mol SO2和0.20mol O2,等效为增大压强,平衡向正反应移动,二氧化硫的转化率增大,n(SO3)的极小值为0.18mol× =0.36mol,反应为可逆反应,假定完全反应n(SO3)的极大值为0.4mol,故0.36mol<n(SO3)<0.4mol,
=0.36mol,反应为可逆反应,假定完全反应n(SO3)的极大值为0.4mol,故0.36mol<n(SO3)<0.4mol,
故答案为:0.036,0.36mol<n(SO3)<0.4mol.
点评:题目综合性较大,涉及化学平衡影响因素及计算、反应热、溶度积、溶液酸碱性判断、电离平衡常数计算等,是对知识的综合运用,注意(4)中运用等效思想与极值法进行范围的确定.
反应热只与始态与状态有关,催化剂改变平衡建立的途径,不影响始态与终态,反应热不变;
(2)Mg(OH)2、Cu(OH)2的结构类型相同,溶度积越小,溶解度越小,加入相同的浓度的氨水,最先析出;氨水过量,氢氧化铜与氨水反应生成四氨合铜络离子;
(3)根据电荷守恒判断溶液中氢离子与氢氧根离子浓度的相对大小,进而判断溶液的酸碱性;
溶液中存在平衡NH3.H2O?NH4++OH-,根据溶液的pH值计算溶液中c(OH-),根据氯离子浓度计算c(NH4+),利用物料守恒计算溶液中c(NH3.H2O),代入NH3?H2O的电离常数表达式计算;
(4)根据平衡时三氧化硫的物质的量计算氧气的物质的量变化量,根据v=
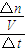 计算v(O2);
计算v(O2);再加入0.20mol SO2和0.10mol O2,等效为开始加入0.40mol SO2和0.20mol O2,等效为增大压强,平衡向正反应移动,二氧化硫的转化率增大,据此确定n(SO3)的极小值,反应为可逆反应,假定完全反应确定n(SO3)的极大值.
解答:解:(1)恒温恒压条件下向平衡体系中通入氩气,体积增大,等效为降低压强,平衡向体积增大的方向移动,该反应正反应是体积减小的反应,故平衡向左移动.
反应热只与始态与状态有关,催化剂改变平衡建立的途径,不影响始态与终态,反应热不变,
故答案为:作,不改变;
(2)Mg(OH)2、Cu(OH)2的结构类型相同,Cu(OH)2溶度积更小,溶解度越小,加入相同的浓度的氨水,Cu(OH)2最先析出,反应离子方程式为:Cu2++2NH3.H2O=Cu(OH)2↓+2NH4+,氨水过量,氢氧化铜与氨水反应生成四氨合铜络离子,离子方程式为:Cu(OH)2+4NH3.H2O=[Cu(NH3)4]2++2OH-+4H2O,
故答案为:Cu2++2NH3.H2O=Cu(OH)2↓+2NH4+,Cu(OH)2+4NH3.H2O=[Cu(NH3)4]2++2OH-+4H2O;
(3)根据电荷守恒有c(NH4+)+c(H+)=c(Cl-)+c(OH-),由于c(NH4+)=c(Cl-),故c(H+)=c(OH-),溶液呈中性,故溶液中c(OH-)=10-7mol/L,溶液中c(NH4+)=c(Cl-)=
 ×0.01mol?L-1=0.005mol?L-1,故混合后溶液中c(NH3.H2O)=
×0.01mol?L-1=0.005mol?L-1,故混合后溶液中c(NH3.H2O)= ×amol?L-1-0.005mol?L-1=(0.5a-0.005)mol/L,NH3?H2O的电离常数Kb=
×amol?L-1-0.005mol?L-1=(0.5a-0.005)mol/L,NH3?H2O的电离常数Kb=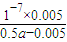 =
=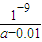 ,
,故答案为:中,
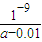 ;
;(4)平衡时三氧化硫的物质的量为0.18mol,由方程式可知,氧气的物质的量变化量为0.18mol×
 =0.09mol,所以v(O2)=
=0.09mol,所以v(O2)= =0.036mol/(L?min),
=0.036mol/(L?min),再加入0.20mol SO2和0.10mol O2,等效为开始加入0.40mol SO2和0.20mol O2,等效为增大压强,平衡向正反应移动,二氧化硫的转化率增大,n(SO3)的极小值为0.18mol×
 =0.36mol,反应为可逆反应,假定完全反应n(SO3)的极大值为0.4mol,故0.36mol<n(SO3)<0.4mol,
=0.36mol,反应为可逆反应,假定完全反应n(SO3)的极大值为0.4mol,故0.36mol<n(SO3)<0.4mol,故答案为:0.036,0.36mol<n(SO3)<0.4mol.
点评:题目综合性较大,涉及化学平衡影响因素及计算、反应热、溶度积、溶液酸碱性判断、电离平衡常数计算等,是对知识的综合运用,注意(4)中运用等效思想与极值法进行范围的确定.

练习册系列答案
 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案
相关题目
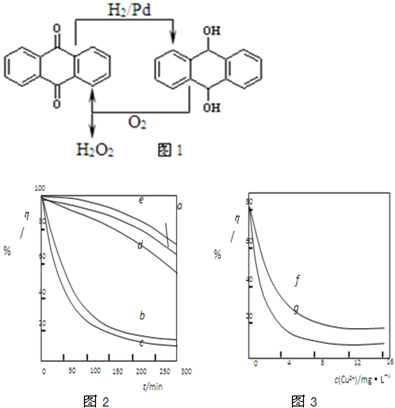
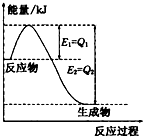 运用化学反应原理研究氮、氯、碘等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、氯、碘等单质及其化合物的反应有重要意义.