题目内容
在一密闭容器中盛有2molNa2O2与2molNaHCO3,将其加热到150℃,经充分反应后,容器内残留的固体是 ( )
| A.1molNa2CO3和2molNaOH | B.2molNa2CO3和2molNaOH |
| C.2molNa2CO3和1molNa2O2 | D.只有2molNa2CO3 |
B
解析试题分析:碳酸氢钠首先分解,2NaHCO3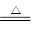 Na2CO3+H2O+CO2↑。由于氢氧化钠能和CO2反应生成碳酸钠和水,所以过氧化钠先与二氧化碳反应,后与水反应,即2Na2O2+2CO2=2Na2CO3+O2、2Na2O2+2H2O=4NaOH+O2↑。2mol碳酸氢钠分解生成水和二氧化碳均为1mol,过氧化钠为2mol,所以水、二氧化碳、过氧化钠恰好完全反应。最终残留固体为2mol碳酸钠、2mol氢氧化钠,答案选B。
Na2CO3+H2O+CO2↑。由于氢氧化钠能和CO2反应生成碳酸钠和水,所以过氧化钠先与二氧化碳反应,后与水反应,即2Na2O2+2CO2=2Na2CO3+O2、2Na2O2+2H2O=4NaOH+O2↑。2mol碳酸氢钠分解生成水和二氧化碳均为1mol,过氧化钠为2mol,所以水、二氧化碳、过氧化钠恰好完全反应。最终残留固体为2mol碳酸钠、2mol氢氧化钠,答案选B。
考点:考查过氧化钠和碳酸氢钠混合加热的有关计算
点评:该题是中等难度的试题,试题基础性强,注重能力的培养的解题方法的指导。该题的关键是明确在有水和CO2同时存在的条件下,过氧化钠与之反应的先后顺序。有助于培养学生的发散思维能力和抽象思维能力。该题也可以通过原子守恒进行逐一排除得到。

练习册系列答案
相关题目
|
在一密闭容器中盛有2 mol Na2O2与2 mol NaHCO3,将其加热到150℃,经充分反应后,容器内残留的固体是 | |
| [ ] | |
A. |
1 mol Na2CO3和2 mol NaOH |
B. |
2 mol Na2CO3和2 mol NaOH |
C. |
2 mol Na2CO3和1 mol Na2O2 |
D. |
只有2 mol Na2CO3 |